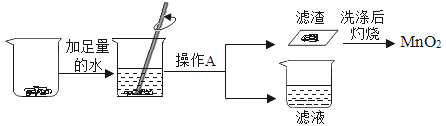
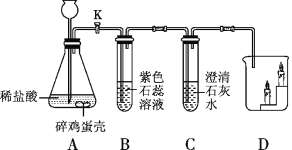
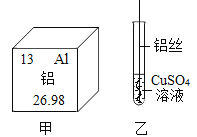
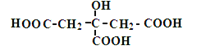题目内容
【题目】(每空1分,共10分)
(1)用化学用语(即化学符号)填空:
两个氧原子: ;保持氢气化学性质的粒子是: 。
(2)说出下列符号中数字“2”的意义:
![]() : ;
: ;![]() : 。
: 。
(3)等质量的①O2;②CO2;③CO;④SO2中所含分子数由多到少的顺序是 (填序号)。
(4)如下图所示,“○”、“●”表示两种不同的原子,其中表示单质的是 (填序号,下同)。可能是氧化物的是 。
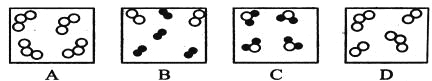
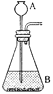
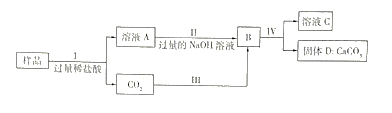
(5)甲、乙、丙三种物质均含地壳中含量最多的元素。甲、乙是组成元素相同的化合物,丙是单质;甲、乙在常温下均为液体,在一定条件下均可分解生成丙;它们之间有如图所示的转化关系(部分物质和反应条件已经略去)。
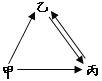
则:甲的化学式为 ;乙转化成丙的文字表达式为 ;从微观的角度解释甲、乙性质有差异的原因是 。
【答案】2O; H2; 每个氧分子中含有2个氧原子; 每个亚铁离子带2个单位的正电荷; ③①②④。 A; C; H2O2; 水![]() 氢气+氧气; 分子构成不同。
氢气+氧气; 分子构成不同。
【解析】
(1)两个氧原子先写数量再写符号,表示为2O;氢分子是保持氢气化学性质的粒子,表示为H2;
(2)O2中右下角的2表示每个氧分子中含有2个氧原子;Fe2+中右上角的2表示每个亚铁离子带2个单位的正电荷;
(3)等质量的氧气、二氧化碳、一氧化碳、二氧化硫比较分子数量多少时,可比较各物质的相对分子质量,相对分子质量越大,等质量时分子数越小,根据计算,氧气相对分子质量为32,二氧化碳相对分子质量为44,一氧化碳相对分子质量为28,二氧化硫相对分子质量为64,故分子数由多到少的顺序是③①②④;
(4)单质由一种元素组成的纯净物,根据微观示意图可知,A为单质;氧化物是由两种元素组成的纯净物,其中一种元素为氧元素,由图可知,C可能为氧化物。
(5)地壳中含量最多的元素为氧元素,故甲乙丙三种物质中均有氧元素,又因为丙是单质,故丙是氧气,甲、乙在常温下均为液体且甲、乙是组成元素相同的化合物故甲乙是水和过氧化氢,根据示意图可知甲能生成乙,故甲是过氧化氢,化学式为H2O2,乙是水。乙转化成丙的文字表达式为水![]() 氢气+氧气,甲和乙性质有差异是因为分子是保持物质化学性质的最小粒子,甲乙的分子构成不同。
氢气+氧气,甲和乙性质有差异是因为分子是保持物质化学性质的最小粒子,甲乙的分子构成不同。

 阅读快车系列答案
阅读快车系列答案