题目内容
【题目】根据所学的知识并结合下列仪器,回答有关问题:

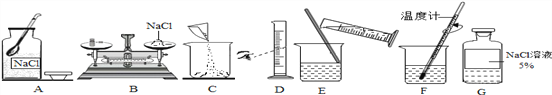
(1)写出仪器的名称B ,C 。
(2)实验室以氯酸钾为原料制取并收集氧气,完成这个实验除选用A、D、E、F,I外,还需增加的仪器是 ,反应的化学方程式为 。
(3)实验室用 为原料(填两种原料名称)来制取二氧化碳,组装一套发生装置所需的仪器 (填字母)。
(4)实验室还用Zn和稀H2SO4来制取氢气,反应的化学方程式为 。
(5)某同学制作的微型实验装置(夹持仪器略)。甲酸与热的浓硫酸反应的方程式为:![]()
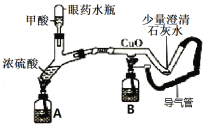
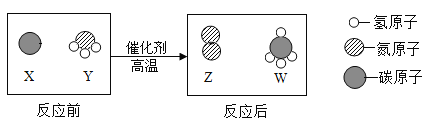
①则X是 (填化学式);
②实验开始时先要点燃A处酒精灯一段时间后,再点燃B处酒精的目的是 。
③此实验装置的主要优点是 。
【答案】(1)B的名称 锥形瓶;C的名称 长颈漏斗
(2)增加的仪器 酒精灯;方程式2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
(3)制取二氧化碳的原料 大理石稀盐酸;发生装置的仪器 AH、BH、ACG、BCG。
(4)制取氢气的反应方程式Zn+H2SO4==ZnSO4+H2↑
(5)①H2O ②排尽装置内空气,防炸。
③减少污染和节约资源
【解析】
试题分析:(2)根据反应物的状态和反应条件选择发生装置,用氯酸钾和二氧化锰制取氧气属固固加热型,氧气的密度比空气大,难溶于水,故用向上排空气法或排水法收集。故需要增加的仪器是酒精灯。氯酸钾分解生成的是氯化钾和氧气:2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
(3)实验室用石灰石和稀元素反应制取二氧化碳,故固液在常温下的反应;二氧化碳的密度比空气大,易溶于水,故用向上排空气法收集氧气。需要的仪器有:锥形瓶、长颈漏斗、双孔橡皮塞,集气瓶、玻璃片;
(4)实验室用锌和稀硫酸反应制取氢气的同时还生成了硫酸锌:Zn+H2SO4==ZnSO4+H2↑;
(5)①根据质量守恒定律化学反应前后原子的种类和数目不变,反应前C:1,H:2,O:2,反应后C:1,H:0,O:1,故X的化学式为H2O;
②一氧化碳具有可燃性,若不纯可能会发生爆炸,故要先把玻璃管中的空气排尽再加热;
③该装置中的眼药水瓶相当与分液漏斗,能控制滴加的药品的量并能节约药品;该装置有尾气处理装置,不会污染空气。

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案