题目内容
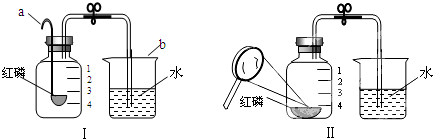
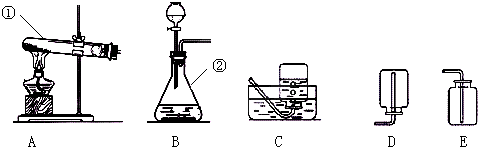
下列实验操作中,能达到实验目的的是
- A.检验氢气的纯度时,没有听到任何响声,表明氢气已纯净
- B.用适量的水区分硝酸铵固体和氢氧化钠固体
- C.粗盐提纯实验中,蒸发结晶直接滤液蒸干时停止加热
- D.用PH试纸测定溶液酸碱度时,先将PH试纸用水润湿,然后再测定
B
A、点燃气体时,发出尖锐爆鸣声表示氢气不纯,声音很小则表示氢气较纯,没有听到任何声响,也可能没有收集到氢气,故A错误,
B、硝酸铵溶于水,溶液温度降低,氢氧化钠溶于水,溶液温度升高,根据温度的不同可以区分,故B正确,
C、待蒸发皿中出现较多固体时,停止加热,滤液蒸干会造成氯化钠晶体的飞溅,故C错误,
D、pH试纸用水湿润后后,会稀释待测的溶液,使测得的pH值不准确,故D错误,
故选B.
A、点燃气体时,发出尖锐爆鸣声表示氢气不纯,声音很小则表示氢气较纯,没有听到任何声响,也可能没有收集到氢气,故A错误,
B、硝酸铵溶于水,溶液温度降低,氢氧化钠溶于水,溶液温度升高,根据温度的不同可以区分,故B正确,
C、待蒸发皿中出现较多固体时,停止加热,滤液蒸干会造成氯化钠晶体的飞溅,故C错误,
D、pH试纸用水湿润后后,会稀释待测的溶液,使测得的pH值不准确,故D错误,
故选B.

练习册系列答案
相关题目
(2010?达州)纯碱(Na2CO3)是一种重要的盐类物质,在化学工业中用途极广.工业上通常用氨碱法来生产.小红同学为探究纯碱的化学性质进行了猜想,并设计实验进行验证.请你帮助她将下列实验报告填写完整.
[交流与反思]若用稀硫酸代替稀盐酸进行实验,是否与猜想二相同?______(填“是”或“否”).
| 猜想 | 实验操作 | 实验现象 | 结论(或化学方程式) |
| 猜想一:Na2CO3溶液显碱性 | 取少量的Na2CO3溶液试管中,滴入2-3滴酚酞试液,振荡 | ______ | 溶液显碱性 |
| 猜想二:能与酸反应 | 取少量的Na2CO3溶液试管中,然后滴加稀盐酸 | 有大量的气泡 | 化学方程式:______ |
| 猜想三:能与Ca(OH)2反应 | 向盛有少量Na2CO3溶液的试管中滴加澄清石灰水 | 出现白色沉淀 | 化学方程式:______ |
| 猜想四:能与氯化钡反应 | ______ | 出现白色沉淀 | Na2CO3+BaCl2=BaCO3↓+2NaCl 反应的基本类型为:______ |