题目内容
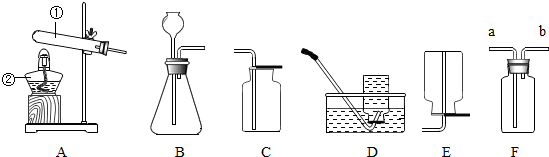
某兴趣小组的几位同学在实验室用下列装置制取气体.

(1)写出图中标有①、②的仪器名称:①______②______;
(2)采用B装置制取氧气时,锥形瓶中放入的物质(写名称)是______,长颈漏斗中加入的物质(写化学式)是______,写出该反应的文字表达式:______,收集氧气时可用D装置,也可用F装置,用F装置收集氧气时,气体应从______(填a或b)管通入;
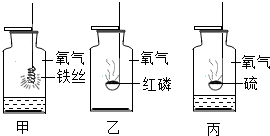
(3)氧气是一种化学性质比较活泼的气体,它可以和许多物质发生反应,如下图所示:

上述三个反应的相同点有______(多选,填序号)
A.都是化合反应 B.都是氧化反应 C.都是非金属与氧气反应
D.都需要点燃或加热 E.都是金属与氧气反应
(4)做甲实验时,事先需在集气瓶中装有少量水,其作用是______.
(5)大量的实验证明,红磷、硫、木炭等在氧气中燃烧比在空气中燃烧剧烈;做实验甲时,铁丝在氧气中剧烈燃烧,而在空气中只是发红并未燃烧.据此,说明可燃物能否燃烧或燃烧的剧烈程度与______有关.
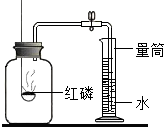
(6)将装置乙改装为下图所示装置还可用于测定空气中氧气的体积分数:
 经测定,集气瓶的容积为250ml,在此实验中,观察到量筒中减少的水的体积为50ml,则空气中氧气的体积分数为______.实验需保证整个装置不漏气且所用红磷必须足量,如果实验时未冷却到室温便打开弹簧夹观察量筒内减少的水的体积,则实验结果将(填偏大、偏小或不变)______.实验完毕后,集气瓶内残余的气体主要是______(填化学符号).若将上述实验中的红磷换成木炭(其他不变)进行实验,并未发现倒吸现象,其原因是______.
经测定,集气瓶的容积为250ml,在此实验中,观察到量筒中减少的水的体积为50ml,则空气中氧气的体积分数为______.实验需保证整个装置不漏气且所用红磷必须足量,如果实验时未冷却到室温便打开弹簧夹观察量筒内减少的水的体积,则实验结果将(填偏大、偏小或不变)______.实验完毕后,集气瓶内残余的气体主要是______(填化学符号).若将上述实验中的红磷换成木炭(其他不变)进行实验,并未发现倒吸现象,其原因是______.
反思此实验的探究过程,用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是(答一条)______.
解:(1)根据图中制取氧气的装置,写出常用仪器名称:①试管 ②酒精灯
(2)用过氧化氢溶液制取氧气的装置不要加热装置,所以采用B装置;根据氧气的密度大于空气和难溶于水的性质选择收集装置.
(3)氧气与磷、硫、铁丝的文字表达式:氧气+铁丝 四氧化三铁,氧气+磷
四氧化三铁,氧气+磷 五氧化二磷,氧气+硫
五氧化二磷,氧气+硫 二氧化硫.根据文字表达式,归纳总结三个化学反应的相同点.
二氧化硫.根据文字表达式,归纳总结三个化学反应的相同点.
(4)总结归纳氧气与磷、硫、铁丝的反应现象及注意事项.
(5)氧化反应的剧烈程度,与反应物的性质和反应物的浓度等有关.
(6)空气中氧气的体积分数为:①50ml÷250ml=20%,②未冷却到室温,集气瓶内的热气体的压强较大,③空气主要成分氧气被消耗,则剩余氮气,④木炭燃烧消耗氧气,生成二氧化碳,瓶内气体体积无明显减小,压强变化不大,所以并未发现倒吸现象.
故答为:(1)①试管 ②酒精灯
(2)二氧化锰 H2O2过氧化氢 水+氧气 a
水+氧气 a
(3)A、B、D
(4)防止熔化物溅落到瓶底,炸裂瓶底
(5)氧气的浓度(意思对即可)
(6)20% 偏小 N2木炭燃烧消耗氧气,同时生成二氧化碳,瓶内气体体积无明显减小 药品只与氧气反应(生成物最好是固体)等.
分析:(1)如图所示制取氧气的装置,写出常用仪器名称;
(2)用过氧化氢溶液制取氧气的装置不要加热装置,所以采用B装置;根据氧气的密度大于空气和难溶于水的性质选择收集装置.
(3)氧气与磷、硫、铁丝的文字表达式:氧气+铁丝 四氧化三铁,氧气+磷
四氧化三铁,氧气+磷 五氧化二磷,氧气+硫
五氧化二磷,氧气+硫 二氧化硫.根据文字表达式,归纳总结三个化学反应的相同点.
二氧化硫.根据文字表达式,归纳总结三个化学反应的相同点.
(4)总结归纳氧气与磷、硫、铁丝的反应现象及注意事项.
(5)氧化反应的剧烈程度,与反应物的性质和反应物的浓度等有关.
(6)①量筒中减少的水的体积为50ml,即为集气瓶中消耗氧气的体积,则可算空气中氧气的体积分数;②未冷却到室温,集气瓶内的热气体的压强较大,打开弹簧夹观察量筒内减少的水的体积将较小;③空气主要成分为:氧气和氮气,氧气被消耗,剩余氮气;④木炭燃烧消耗氧气,同时生成二氧化碳,瓶内气体体积无明显减小,压强变化不大,所以并未发现倒吸现象.
点评:(1)此题重在考查同学们对常用化学仪器的了解和识记情况,只有很好的认识它们,做实验才能得心应手.
(2)本题是对测定空气里氧气的含量的以及实验操作的注意事项的探究.
(2)用过氧化氢溶液制取氧气的装置不要加热装置,所以采用B装置;根据氧气的密度大于空气和难溶于水的性质选择收集装置.
(3)氧气与磷、硫、铁丝的文字表达式:氧气+铁丝
 四氧化三铁,氧气+磷
四氧化三铁,氧气+磷 五氧化二磷,氧气+硫
五氧化二磷,氧气+硫 二氧化硫.根据文字表达式,归纳总结三个化学反应的相同点.
二氧化硫.根据文字表达式,归纳总结三个化学反应的相同点.(4)总结归纳氧气与磷、硫、铁丝的反应现象及注意事项.
(5)氧化反应的剧烈程度,与反应物的性质和反应物的浓度等有关.
(6)空气中氧气的体积分数为:①50ml÷250ml=20%,②未冷却到室温,集气瓶内的热气体的压强较大,③空气主要成分氧气被消耗,则剩余氮气,④木炭燃烧消耗氧气,生成二氧化碳,瓶内气体体积无明显减小,压强变化不大,所以并未发现倒吸现象.
故答为:(1)①试管 ②酒精灯
(2)二氧化锰 H2O2过氧化氢
 水+氧气 a
水+氧气 a(3)A、B、D
(4)防止熔化物溅落到瓶底,炸裂瓶底
(5)氧气的浓度(意思对即可)
(6)20% 偏小 N2木炭燃烧消耗氧气,同时生成二氧化碳,瓶内气体体积无明显减小 药品只与氧气反应(生成物最好是固体)等.
分析:(1)如图所示制取氧气的装置,写出常用仪器名称;
(2)用过氧化氢溶液制取氧气的装置不要加热装置,所以采用B装置;根据氧气的密度大于空气和难溶于水的性质选择收集装置.
(3)氧气与磷、硫、铁丝的文字表达式:氧气+铁丝
 四氧化三铁,氧气+磷
四氧化三铁,氧气+磷 五氧化二磷,氧气+硫
五氧化二磷,氧气+硫 二氧化硫.根据文字表达式,归纳总结三个化学反应的相同点.
二氧化硫.根据文字表达式,归纳总结三个化学反应的相同点.(4)总结归纳氧气与磷、硫、铁丝的反应现象及注意事项.
(5)氧化反应的剧烈程度,与反应物的性质和反应物的浓度等有关.
(6)①量筒中减少的水的体积为50ml,即为集气瓶中消耗氧气的体积,则可算空气中氧气的体积分数;②未冷却到室温,集气瓶内的热气体的压强较大,打开弹簧夹观察量筒内减少的水的体积将较小;③空气主要成分为:氧气和氮气,氧气被消耗,剩余氮气;④木炭燃烧消耗氧气,同时生成二氧化碳,瓶内气体体积无明显减小,压强变化不大,所以并未发现倒吸现象.
点评:(1)此题重在考查同学们对常用化学仪器的了解和识记情况,只有很好的认识它们,做实验才能得心应手.
(2)本题是对测定空气里氧气的含量的以及实验操作的注意事项的探究.

练习册系列答案
相关题目
 经测定,集气瓶的容积为250mL,在此实验中,观察到量筒中减少的水的体积为50mL,则空气中氧气的体积分数为
经测定,集气瓶的容积为250mL,在此实验中,观察到量筒中减少的水的体积为50mL,则空气中氧气的体积分数为 A题:小明从某食品包装袋中取出一小包物质,部分标签如图:
A题:小明从某食品包装袋中取出一小包物质,部分标签如图:
