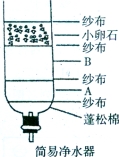
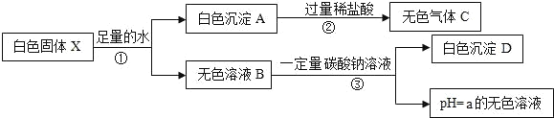
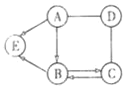
��Ŀ����
����Ŀ����ͼ�м���A��B��C���ֹ������ʵ��ܽ������ͼ��
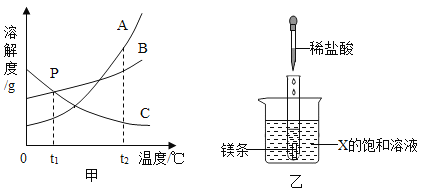
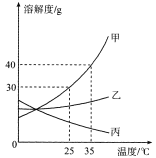
��1����ͼ�У�t2 ��ʱ��A��B��C���������У��ܽ��������_____��P������ʾ�ĺ���Ϊ_________��
��2��t2 ��ʱ��Ҫ��A��B��C�������ʵı�����Һ�У�������ͬ�����ľ��壬������������ܼ��������ɴ�С��˳����_________��
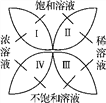
��3����ͼ����ʾ��20 ��ʱ�����Թܷ���ʢ��X�ı�����Һ���ձ��У����Թ��м���þ�����ټ���5 mLϡ���ᣬ�����������������ݣ�ͬʱ�ձ��б���ǣ���X����ΪA��B��C���ֹ��������е���һ�֣�________��
���𰸡�A t1 ��ʱ������B��C���ܽ����� C>B>A C
��������
��1����ͼ��֪��t2��ʱ���������ʵ��ܽ�ȴ�С˳��Ϊ��A��B��C��P����t1��ʱ��B�� C���ܽ�����ߵĽ��㣬������ĺ�����t1��ʱ��B��C���ܽ����ȡ��ʴ�Ϊ��A��t1��ʱ������B��C���ܽ����ȣ�
��2����ͼ��֪��t2��ʱ���������ʵ��ܽ�ȴ�С˳��Ϊ��A��B��C����������ͬ���������ʣ�����Ҫ���ܼ��������ɴ�СΪ��C��B��A������Ҫ������ͬ�����ľ��壬����Ҫ�������ܼ��������ɴ�С��˳��ҲΪ��C��B��A���ʴ�Ϊ��C��B��A��
��3��þ��ϡ���ᷴӦ�����Ȼ�þ���������÷�Ӧ��һ�����ȷ�Ӧ������ʱ�۲쵽�ձ��б���ǣ���֤����Һ���о�������������Է�����������Һ�����ʵ��ܽ�ȣ����¶ȵ����߶����͡�ͼ���У�A��B�������ʵ��ܽ�����¶ȵ����߶�����C���ܽ�����¶ȵ����߶����͡�����������C���ʴ�Ϊ��C��

 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д� ��ѧ�̸̳����¿α�ϵ�д�
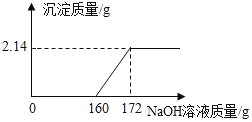
��ѧ�̸̳����¿α�ϵ�д�����Ŀ����ˮƿ��ˮ������Ҫ�ɷ���Mg��OH��2��CaCO3����������������ϴ��ȥ��С��Ϊ�ⶨˮ����̼��Ƶ���������������������ʵ�飺ȡ200gˮ������������μ���������ϡ���ᣬ�����������建��ͨ����������������Һ�У�ͬʱ����8min������������Һ�����ı仯ֵ�����ý�����±���ʾ������ϡ����Ļӷ�����
ʱ�䣨min�� | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
����������Һ���ӵ�������g�� | 0 | 13 | 24 | 32 | 31 | 41 | 43 | 44 | 44 |
��1��������һ��ʱ�������������������Һ���ӵ������������Ǵ���ģ���ʱ���ǵ�__min��
��2��200gˮ����������ϡ�����У�����CO2���������Ϊ______g��
��3������ˮ����̼��Ƶ�����������________
��4��������ͼ����ͼ������ȷ��������������������Һ���ӵ�������ʱ��ı仯��ϵͼ��__________