题目内容
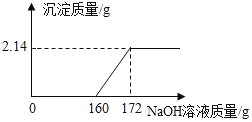
【题目】工业盐酸中通常溶有少量的FeCl3而呈黄色,小红为测定某工业盐酸中HCl的含量进行如下实验:取某工业盐酸l00g,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液质量与反应生成的沉淀质量关系如图所示。请回答下列问题:
(1)FeCl3与NaOH恰好完全反应时,生成沉淀的质量是______g。
(2)该工业盐酸中HCl的质量分数是多少(写出计算过程)______________
【答案】2.14g29.2%
【解析】
(1)由图可知,完全反应后生成沉淀的质量为2.14g;
(2)由图可知,与氯化铁反应的氢氧化钠溶液的质量为172g-160g=12g;设消耗的氢氧化钠的质量为x,则:
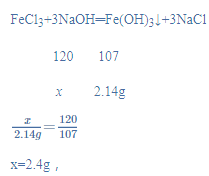
氢氧化钠溶液的溶质质量分数=![]() ×100%=20%,与盐酸反应的氢氧化钠的质量为:160g×20%=32g,设参加反应氯化氢的质量为y,则:
×100%=20%,与盐酸反应的氢氧化钠的质量为:160g×20%=32g,设参加反应氯化氢的质量为y,则:
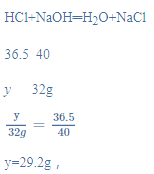
该工业盐酸中HCl的质量分数是:![]() ×100%=29.2%,
×100%=29.2%,
答:(1)FeCl3与NaOH恰好完全反应时,生成沉淀的质量是2.14;(2)该工业盐酸中HCl的质量分数是29.2%。

 口算能手系列答案
口算能手系列答案【题目】金属与人类的生产、生活密切相关,牢固掌握金属的知识十分必要。
(1)下列用途是利用了金属的导电性的是________(填字母代号)。
A.铜作导线 B.金作戒指
C.铝合金作门窗 D.铁锅作炊具
(2)将一小块金属钠放入滴有无色酚酞溶液的水中,钠剧烈反应,可观察到其熔成小球,在水面上游动,溶液变成红色。
①请根据上述现象总结金属钠的物理性质(写出两点即可)_________________。
②已知该反应还产生了一种可燃性气体,请写出此反应的化学方程式_______________。
(3)将锌粉加到含有 Cu(NO3)2 和 AgNO3 的混合溶液中,充分反应后过滤。
①若滤液中只含有一种溶质,请分析滤渣的成分_______________。
②若滤渣中含有两种金属,请分析滤液的成分_______________。
(4)合金的种类很多,用途十分广泛,黄铜是铜和锌的合金,它可以用来制造机器和电器的零件等,化学兴趣小组的同学欲测定某铜样品中铜的质量分数(不考虑黄铜中的其他杂质),请你参与他们的探究过程。称量 10 g 粉末状黄铜样品放入烧杯中,量取 45 mL 稀盐酸分三次加入其中,每次充分反应后,测定生成氢气的质量,实验数据如表:
第一次 | 第二次 | 第三次 | |
加入稀盐酸的体积(mL) | 15 | 15 | 15 |
生成氢气的质量(g) | 0.04 | m | 0.02 |
试计算:①m 的数值为________。
②此黄铜样品中铜的质量分数是多少__________________
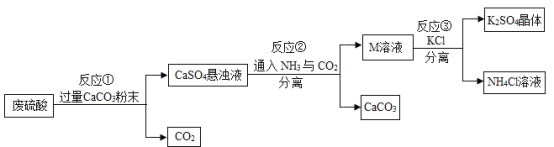
【题目】某化工厂用废硫酸制备K2SO4的流程如下:
物质 | KCl | K2SO4 | NH4Cl | (NH4)2SO4 |
溶解度/g(20℃) | 34.2 | 11.1 | 37.2 | 75.4 |
(1)生产上将CaCO3研成粉末的目的是____________。
(2)上述流程中,除可综合利用CO2外,还可循环使用的物质是____________(填写化学式)。
(3)反应③中相关物质的溶解度如表所示。反应③在常温下 能实现的原因是____________。
(4)洗涤反应③所得晶体不用水而用饱和K2SO4溶液的目的是____________;
检验此晶体是否洗涤干净的方法是____________________________________________________。