题目内容
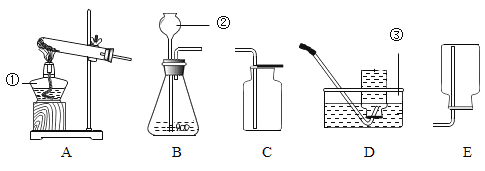
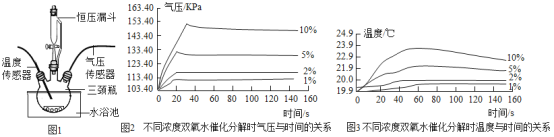
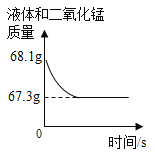
【题目】化学兴趣小组用一瓶久 置的过氧化氢溶液制取氧气并测量过氧化氢质量分数。称量68g过氧化氢溶液和0.1g二氧化锰进行实验,反应前后液体和二氧化锰的质量随时间变化关系如下图。
计算:
(1)反应生成氧气的质量______?
(2)参加反应的过氧化氢的质量____________?
【答案】0.8g 1.7g
【解析】
解:由图可知,开始时液体和二氧化锰混合物质量为68.1g,随着反应生成氧气跑掉,混合物质量越来越少,最终保持在67.3g不在减少,说明反应已经结束,此时生成的氧气的质量为68.1g-67.3g=0.8g 设参加反应的过氧化氢质量为x

![]()
x=1.7g
答:(1)制得氧气的质量是 0.8g。 (2)参加反应的过氧化氢质量是1.7g

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
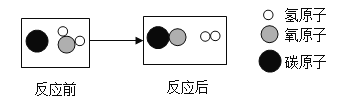
【题目】3.0g某物质完全燃烧后生成4.4gCO2和1.8g水.则对该物质相关判断正确的是( )
| A. | 该物质只含碳、氢元素 |
| B. | 该物质一定含有碳、氢元素,可能含有氧元素 |
| C. | 该物质由碳、氢、氧元素组成 |
| D. | 该物质分子中碳原子和氢原子的个数比为1:1 |