题目内容
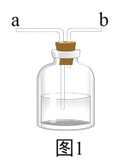
【题目】小丽在实验室发现一瓶氢氧化钠固体没有塞上瓶塞,于是她和同学一起对这瓶氢氧化钠固体是否变质展开探究。
(查阅资料)氯化钙溶液显中性。
(提出问题)这瓶氢氧化钠固体是否变质?
(作出猜想)猜想1:没有变质;猜想2:部分变质;猜想3:_____。
(实验推断)取氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
实验操作 | 实验现象 | 实验结论 |
(1)取少量溶液A于试管中,向其中滴加足量的稀盐酸; | 有气泡产生 | 猜想____不成立 |
(2)另取少量溶液A于试管中,加入过量的氯化钙溶液 | ____ | 反应的化学方程式是____。 |
(3)向(2)所得的滤液中滴入几滴酚酞试液 | 酚酞试液变红 | 证明有_____存在。 |
综合以上实验,说明猜想____成立。 | ||
(反思)因此,氢氧化钠应____保存。
【答案】全部变质 1 有白色沉淀产生 CaCl2+Na2CO3=CaCO3↓+2NaCl 氢氧化钠 2 密封
【解析】
猜想1为没有变质,猜想2为部分变质,则猜想3应该为全部变质;
(1)取少量溶液A于试管中,向其中滴加足量的稀盐酸有气泡产生,说明氢氧化钠已经发生了变质,则猜想1不成立;
(2)氢氧化钠变质产生碳酸钠,则另取少量溶液A于试管中,加入过量的氯化钙溶液,生成碳酸钙白色沉淀;
反应的化学方程式为CaCl2+Na2CO3=CaCO3↓+2NaCl;
(3)向(2)所得的滤液中滴入几滴酚酞试液,酚酞试液变红,说明滤液呈碱性;而因为氯化钙过量则滤液中不存在碳酸钠,且氯化钙为中性,则该碱性溶液只能是氢氧化钠;
以上实验说明样品中既有氢氧化钠也有碳酸钠,则说明该样品部分变质,故猜想2正确;
由此可得出的结论是氢氧化钠应该密封保存,避免和二氧化碳反应使其变质。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列四个图像中,能正确反映对应变化关系的是( )
|
|
|
|
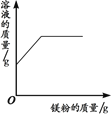
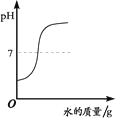
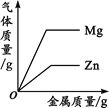
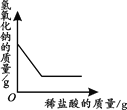
A.向一定量的稀盐酸中加入过量的镁粉 | B.向一定量的稀盐 | C.向两份完全相同的稀盐酸中分别加入锌粉、镁粉 | D.向一定量氢氧化钠溶液中滴加稀盐酸 |
A. AB. BC. CD. D