��Ŀ����
����Ŀ��ij��ȤС������п����ϡ���ᷴӦ��ʵ�����Ũ�������ϡ������п������ʵ�飬�д̼�����ζ���������Ϊ����֤������ijɷ֣���С��ͨ���������ϵ�֪��Ũ������ǿ�����ԣ�����������ʷ�Ӧ��SO2��ʹƷ����Һ��ɫ���ɱ�����KMnO4���գ�����������ʵ�飺

��1��ʵ����ʵ����ۣ�
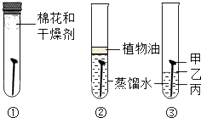
�ٷ�Ӧ���в��ã��۲쵽B�� �� D������������֤��������������SO2 �� д���йط�Ӧ�Ļ�ѧ����ʽ ��
�ڷ�Ӧ��������һ��ʱ���D��������ȼ�գ������ձ��ڱ���ˮ����֤��������������H2 �� �����������ԭ���� ��
��2����˼�����ۣ�
С����Ϊ����ҵ�Ͽ���п����Ũ���ᷴӦ������ȡ����п��Һ��С����Ϊ�����ˣ�����������
���𰸡�
��1��Ʒ����Һ����ɫ��Zn+2H2SO4��Ũ��=ZnSO4+2H2O+SO2��������Ũ��������ĺ�ˮ�����ɣ�Ũ������ϡ���ᣬϡ�����п��Ӧ��������п������
��2������������Ŀ�����Ⱦ�������������
���������⣺��1����Ũ������ǿ�����ԣ�����������ʷ�Ӧ��SO2��ʹƷ����Һ��ɫ���ɱ�����KMnO4���գ����Է�Ӧ���в��ã��۲쵽B��Ʒ����Һ����ɫ��D������������֤��������������SO2 �� Ũ�����п��Ӧ��������п��ˮ�Ͷ�������ѧ����ʽΪ��Zn+2H2SO4��Ũ��=ZnSO4+2H2O+SO2�����ڷ�Ӧ��������һ��ʱ���D��������ȼ�գ������ձ��ڱ���ˮ����֤��������������H2 �� �����������ԭ���ǣ�����Ũ��������ĺ�ˮ�����ɣ�Ũ������ϡ���ᣬϡ�����п��Ӧ��������п����������2����ҵ�Ͽ���п����Ũ���ᷴӦ������ȡ����п��Һ�������˵������ǣ�����������Ŀ�����Ⱦ�������������
���Դ��ǣ���1��Ʒ����Һ����ɫ��Zn+2H2SO4��Ũ��=ZnSO4+2H2O+SO2����������Ũ��������ĺ�ˮ�����ɣ�Ũ������ϡ���ᣬϡ�����п��Ӧ��������п����������2������������Ŀ�����Ⱦ�������������
�����㾫����������д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ�ǽ����ĸ�������Ҫ֪��ע�⣺a����ƽ b������ c�����ţ�