题目内容
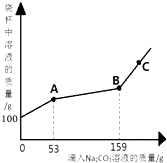
【题目】向一定质量Fe(NO3)2和Cu(NO3)2的混合溶液中加入Zn粉,溶液质量与加入Zn粉的质量关系如图所示.下列说法错误的是( ) 
A.a点溶液中的溶质有3种
B.若取b点溶液,滴加稀盐酸,无白色沉淀
C.取c点的固体,加入稀盐酸,无气泡产生
D.d点溶液中溶质为Zn(NO3)2
【答案】C
【解析】解:在金属活动性顺序中,Zn>Fe>Cu,向一定质量Fe(NO3)2和Cu(NO3)2的混合溶液中加入Zn粉,与两种溶质依次发生反应
Zn+Fe(NO3)2=Zn(NO3)2+ | Fe |
65 | 56 |
所以析出铁的过程是溶液质量增加的过程;
Zn+Cu(NO3)2=Zn(NO3)2+ | Cu |
65 | 64 |
所以析出铜的过程是溶液质量增加的过程,
A、在a点时,硝酸铜没有全部参加反应,溶液中含有硝酸亚铁、硝酸铜和生成的硝酸锌,溶质是三种,故A正确;
B、b~c段是硝酸铜全部参加反应完后锌和硝酸铜反应的过程,因此滴加稀盐酸,不会产生沉淀,故B正确;
C、c点时锌和硝酸亚铁反应的过程,因此滴加稀盐酸,生成了铁,有气泡产生,故C错误;
D、d点时锌过量,溶液中只有硝酸锌,故D正确.
故选:C.
【考点精析】关于本题考查的金属材料的选择依据,需要了解黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属才能得出正确答案.

【题目】为了测定某石灰石样品中碳酸钙的含量,小敏同学取12.5g该样品进行实验,然后将100mL稀盐酸分五次加入该样品中,充分反应后测得每次生成气体的质量如下表所示(样品中的杂质不反应,生成的气体全部逸出).
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀盐酸的体积/mL | 20 | 20 | 20 | 20 | 20 |
生成气体的质量/g | 1.1 | 1.1 | 1.1 | 1.1 | 0 |
请计算:
(1)生成气体的总质量是g.
(2)碳酸钙(CaCO3)的化学式量是 .
(3)该石灰石样品中碳酸钙的质量分数(写出计算过程).