题目内容
【题目】随着环保和能源问题的日益严重,生产过程中原料的综合利用、节能减排问题正日益被人们所重视。某化工厂为综合利用生产过程中的副产品CaSO4而与相邻的化肥厂联合设计的制(NH4)2SO4的工艺流程如下。
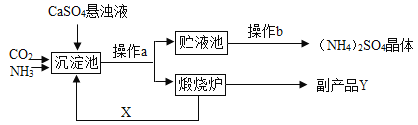
(1)操作b的名称是____________。
(2)X循环使用有利于节能减排、降低生产成本,X是______,副产品Y是________ 。
(3)为促进CO2的溶解吸收,应先向沉淀池中通入NH3,再通入CO2。沉淀池中发生的主要化学反应方程式为________。
(4)判断(NH4)2SO4化肥中有无NH4HCO3的方法:取少量式样溶于水,滴加足量的________,若出现_________,则可判断该化肥中不存在NH4HCO3。
(5)从绿色化学和资源综合利用的角度,说明上述流程的主要优点是_________。
【答案】蒸发结晶 二氧化碳 氧化钙 CO2+2NH3+CaSO4+H2O=CaCO3↓+(NH4)2SO4 稀盐酸 无明显现象 循环使用,得到的产品和副产品都是有用的物质,无废物的产生
【解析】
二氧化碳和氨气和硫酸钙和水生成碳酸钙和硫酸铵,稀盐酸和碳酸氢铵反应生成氯化铵、二氧化碳和水。
(1)贮液池中是硫酸铵溶液,由于不含其它杂质,而硫酸铵也不带结晶水,所以可以蒸发掉水分得到硫酸铵晶体,操作b的名称为蒸发结晶。
(2)X循环使用有利于节能减排、降低生产成本,X是碳酸钙高温煅烧的产物,且在前面反应物中出现过,X是CO2,而同时生成的氧化钙,则是副产品,故X是二氧化碳,副产品Y是氧化钙。
(3)为促进CO2的溶解吸收,应先向沉淀池中通入NH3,再通入CO2,沉淀池中进入的物质也就是反应物为二氧化碳、氨气和硫酸钙以及水,生成物为碳酸钙和硫酸铵,沉淀池中发生的主要化学反应为CO2+2NH3+CaSO4+H2O=CaCO3↓+( NH4)2SO4。
(4)判断(NH4)2SO4化肥中有无NH4HCO3的存在,是区别或者鉴别碳酸氢根离子的存在,如加入稀盐酸生成气体有气泡产生,则说明硫酸铵中含有碳酸氢铵,稀盐酸和碳酸氢铵反应生成氯化铵、二氧化碳和水,二氧化碳气体逸出产生气泡。由于给出了结论是不存在碳酸氢铵,所以对应的现象是没有气泡,故方法为取少量样品溶于水,滴加足量的稀盐酸,若出现无明显现象,则可判断该化肥中不存在NH4HCO3。
(5)原料本身来自生产过程中的副产品CaSO4,而过程中生成的二氧化碳被收回利用,生成物都是可利用的物质,无废物、废气产生,所以从绿色化学和资源综合利用的角度说明上述流程的主要优点是循环使用,得到的产品和副产品都是有用的物质,无废物的产生。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案