题目内容
【题目】长期饮用硬水易引起结石病,将硬水煮沸可以得到软水和水垢,水垢的主要成分是CaCO3和Mg(OH)2 , 从水垢中制取氯化钙的主要流程如下: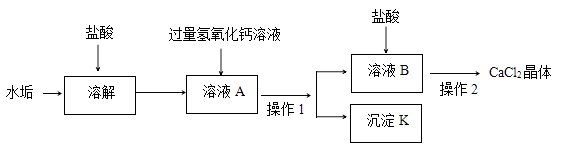
(1)往溶液A加入过量的氢氧化钙溶液,目的是。
(2)操作1的名称是 , 沉淀K是(用化学式表示)。
(3)在溶液B中加入盐酸是为了除去未反应的氢氧化钙,反应的化学方程式是。
【答案】
(1)除去Mg2+和可能过量的H+
(2)过滤;Mg(OH)2
(3)2HCl+ Ca(OH)2 = CaCl2+ 2H2O
【解析】(1)往溶液A加入过量的氢氧化钙溶液,目的是除去Mg2+和可能过量的H+;
(2)操作1的名称是过滤。由(1)知沉淀K是Mg(OH)2;
(3)在溶液B中加入盐酸是为了除去未反应的氢氧化钙,反应的化学方程式是2HCl+ Ca(OH)2 = CaCl2+ 2H2O.
故答案为:(1)除去Mg2+和可能过量的H+;(2)过滤;Mg(OH)2;(3)2HCl+ Ca(OH)2 = CaCl2+ 2H2O.(1)水垢的主要成分是CaCO3和Mg(OH)2。加入盐酸后反应生成氯化钙和氯化镁。加入过量的氢氧化钙会与可能过量的盐酸反应,生成氯化钙和水后,再与氯化镁反应生成氢氧化镁的沉淀;
(2)操作1是固液分离的操作;沉淀K是在氯化镁和氯化钙的混合溶液中加入了过量的氢氧化钙得到的;
(3)盐酸和氢氧化钠生成氯化钙和水.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目