题目内容
【题目】某工厂综合加工海水的主要步骤如图所示.
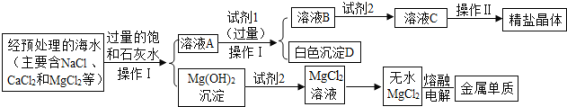
请根据图示回答下列问题:
(1)操作I的名称是_______________。
(2)试剂1是___________________(写化学式,下同),白色沉淀D是____________。
(3)溶液B中含有的溶质是_________________。向溶液B加入试剂2后,在溶液中可观察到_____________的现象。
(4)在熔融状态下电解无水氯化镁会产生一种金属单质和一种双原子分子的气体单质,该反应的化学方程式是_______________________。
【答案】(1) 过滤(2)Na2CO3、CaCO3
(3)NaCl, NaOH, Na2CO3、有气泡产生
(4)MgCl2![]() Mg + Cl2↑
Mg + Cl2↑
【解析】
试题分析:
海水中加入过量的氢氧化钙溶液,氢氧化钙会与氯化镁反应生成氢氧化镁沉淀和氯化钙。通过过滤可将氢氧化镁沉淀除去;滤液A通过处理最终是得到了精盐,故要滤液A中的钙离子除去,故可将过量的碳酸钠。碳酸钠能与氯化钙反应生成碳酸钙沉淀,还能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠。通过过滤可将碳酸钙沉淀除去,那么溶液B中含有碳酸钠、氢氧化钠和氯化钠,氢氧化钠和碳酸钠可通过加稀盐酸除去并得到氯化钠,氯化钠溶液蒸发得到精盐氯化钠。故实际1是碳酸钠,白色沉淀是碳酸钙;电解无水氯化镁会产生一种金属单质和一种双原子分子的气体单质,根据质量守恒定律化学反应前后元素的种类不变可知生成的是氯气,故反应的化学方程式为:MgCl2![]() Mg + Cl2↑。
Mg + Cl2↑。

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目