题目内容
(2009?桂平市二模)现有NaNO3和Na2CO3的混合物20克,为了除去其中的Na2CO3,配制NaNO3溶液,李华同学将该混合物放入一定量的水中配制成60克溶液,再向其中加入50克Ca(NO3)2溶液,恰好完全反应,生成了CaCO3沉淀,过滤后得到100克溶液,计算:(1)生成CaCO3沉淀的质量.
(2)混合物中Na2CO3的质量.
(3)所得溶液中溶质NaNO3的质量分数.
【答案】分析:(1)利用质量守恒定律,由反应前后溶液的质量差计算生成碳酸钙的质量;
(2)根据反应的化学方程式,由生成碳酸钙的质量计算混合物中Na2CO3的质量;
(3)利用所得溶液中溶质NaNO3的质量分数= ×100%求得,其中硝酸钠由原混合物中硝酸钠和反应生成硝酸钠两部分构成,因此还需要根据反应的化学方程式计算生成硝酸钠的质量.
×100%求得,其中硝酸钠由原混合物中硝酸钠和反应生成硝酸钠两部分构成,因此还需要根据反应的化学方程式计算生成硝酸钠的质量.
解答:解:生成CaCO3的质量为:60g+50g-100g=10g
设原混合物中Na2CO3的质量为x,生成NaNO3的质量y.
Na2CO3+Ca(NO3)2=CaCO3↓+2NaNO3
106 100 170
x 10g y
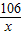 =
= x=10.6g
x=10.6g
 =
=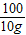 y=17g
y=17g
溶液中NaNO3的总质量=17 g+20 g-10.6 g=26.4 g
溶液中NaNO3的质量分数=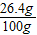 ×100%=26.4%
×100%=26.4%
答:生成CaCO3沉淀的质量为10g;混合物中Na2CO3的质量为10.6g;所得溶液中溶质的质量分数为26.4%
点评:根据反应的化学方程式可以表示反应中各物质的质量比,由反应中任意物质的质量可计算反应中其它物质的质量.
(2)根据反应的化学方程式,由生成碳酸钙的质量计算混合物中Na2CO3的质量;
(3)利用所得溶液中溶质NaNO3的质量分数=
 ×100%求得,其中硝酸钠由原混合物中硝酸钠和反应生成硝酸钠两部分构成,因此还需要根据反应的化学方程式计算生成硝酸钠的质量.
×100%求得,其中硝酸钠由原混合物中硝酸钠和反应生成硝酸钠两部分构成,因此还需要根据反应的化学方程式计算生成硝酸钠的质量.解答:解:生成CaCO3的质量为:60g+50g-100g=10g
设原混合物中Na2CO3的质量为x,生成NaNO3的质量y.
Na2CO3+Ca(NO3)2=CaCO3↓+2NaNO3
106 100 170
x 10g y
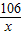 =
= x=10.6g
x=10.6g =
=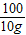 y=17g
y=17g溶液中NaNO3的总质量=17 g+20 g-10.6 g=26.4 g
溶液中NaNO3的质量分数=
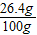 ×100%=26.4%
×100%=26.4%答:生成CaCO3沉淀的质量为10g;混合物中Na2CO3的质量为10.6g;所得溶液中溶质的质量分数为26.4%
点评:根据反应的化学方程式可以表示反应中各物质的质量比,由反应中任意物质的质量可计算反应中其它物质的质量.

练习册系列答案
 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
(2009?桂平市二模)小丽发现自家地里种的花生叶子呈淡黄色,生长迟缓.结合所学的化学知识,小丽给花生施用了碳酸氢铵(NH4HCO3).
发现问题:(1)施用碳酸氢铵两周后,发现效果并不理想.(2)播种花生时,曾向土壤中施用了熟石灰以改良土壤.
搜集资料:(1)碳酸氢铵是______肥(填“氮”“磷”“钾”),花生叶子发黄,选择施用碳酸氢铵是正确的.
(2)含NH4+的盐与碱混合有刺激性气味的氨气产生,氨气的水溶液呈碱性.
(3)碳酸氢铵不稳定,受热易分解.
提出猜想:猜想一:可能是土壤中残留的熟石灰与碳酸氢铵反应使肥效损失.
猜想二:太阳的暴晒,气温的升高也可能使肥效损失.
实验探究:小丽在老师的指导下对碳酸氢铵和熟石灰进行了如下探究.
(1)设计了两种方法证明氢氧化钙溶液的酸碱性,请你帮助她完成探究:
(2)在试管中加热碳酸氢铵和熟石灰的混合物,闻到了刺激性气味,在试管口放一张湿润的红色石蕊试纸,发现试纸变______色,说明有氨气产生.
(3)把少量碳酸氢铵固体放到试管中加热,闻到了刺激性气味,在试管口放一块沾有澄清石灰水的玻璃片,澄清石灰水变浑浊,同时试管口有水滴生成,最后试管中的固体全部消失.请写出反应的化学方程式______ NH3↑+H2O+CO2↑
发现问题:(1)施用碳酸氢铵两周后,发现效果并不理想.(2)播种花生时,曾向土壤中施用了熟石灰以改良土壤.
搜集资料:(1)碳酸氢铵是______肥(填“氮”“磷”“钾”),花生叶子发黄,选择施用碳酸氢铵是正确的.
(2)含NH4+的盐与碱混合有刺激性气味的氨气产生,氨气的水溶液呈碱性.
(3)碳酸氢铵不稳定,受热易分解.
提出猜想:猜想一:可能是土壤中残留的熟石灰与碳酸氢铵反应使肥效损失.
猜想二:太阳的暴晒,气温的升高也可能使肥效损失.
实验探究:小丽在老师的指导下对碳酸氢铵和熟石灰进行了如下探究.
(1)设计了两种方法证明氢氧化钙溶液的酸碱性,请你帮助她完成探究:
| 方 法 | 操 作 | 现象及结论 |
| 方法一 | 取样品于试管中,滴入酚酞试液 | 现象:______; 结论:溶液呈______性. |
| 方法二 | 用______蘸取样品滴在pH试纸上,把试纸呈现的颜色与标准比色卡对照. | 结论:pH______7(填“大于”或“小于”) |
(3)把少量碳酸氢铵固体放到试管中加热,闻到了刺激性气味,在试管口放一块沾有澄清石灰水的玻璃片,澄清石灰水变浑浊,同时试管口有水滴生成,最后试管中的固体全部消失.请写出反应的化学方程式______ NH3↑+H2O+CO2↑