题目内容
【题目】碳酸钡广泛应用于显像管(CRT)、陶瓷、光学玻璃等行业.以碳酸盐矿石(主要成分为 BaCO3和 CaCO3)为原料可生产碳酸钡.
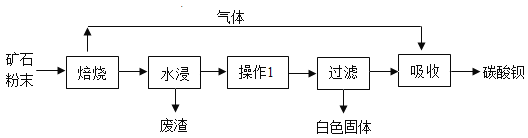
已知碳酸钡和碳酸钙具有相似的化学性质;氧化钡和氧化钙也具有相似的化学性质.氢氧化钙和氢氧化钡在不同温度下的溶解度如下表.
温度/℃ | 0 | 40 | 80 |
Ca(OH)2 溶解度/g | 0.187 | 0.141 | 0.094 |
Ba(OH)2 溶解度/g | 1.67 | 8.22 | 101.4 |
(1)焙烧炉中加入焦炭粉和热空气,焦炭和空气发生反应的作用是________.
(2)生产过程中需要进行多次过滤.实验室进行过滤时,除铁架台(带铁圈)、烧杯和玻璃棒外,还需要的实验用品有________.
(3)“操作 1”是________;通过“操作 1”再过滤,得到的白色固体的化学式为________.
(4)“吸收”中发生的化学反应方程式为________.
【答案】提供热量 漏斗、滤纸 加热(升温) Ca(OH)2 Ba(OH)2 + CO2 = BaCO3↓+ H2O
【解析】
由题目给出的信息可知:焙烧炉中碳酸钡在高温的条件下生成氧化钡和二氧化碳,碳酸钙在高温的条件下生成氧化钙和二氧化碳;氧化钡和水反应生成氢氧化钡,氧化钙和水反应生成氢氧化钙;因此除了水之外,进入“操作1”之前的物质是氢氧化钡和氢氧化钙;“操作1”的方法是:升温、过滤,因为氢氧化钙的溶解度随温度的升高而减小;由溶液制取产品是二氧化碳与氢氧化钡反应生成碳酸钡白色沉淀和水;对矿石进行预处理“研磨成粉状”有利于充分反应;焙烧炉中添加焦炭粉和热空气是为了维持炉内的高温状态;废渣需要经过洗涤才能弃渣,是为了保护环境,同时充分利用原料。
根据以上分析可知:
(1)焙烧炉中加入焦炭粉和热空气,焦炭和空气发生反应的作用是提供热量.
(2)生产过程中需要进行多次过滤,实验室进行过滤时,除铁架台(带铁圈)、烧杯和玻璃棒外,还需要的实验用品有漏斗,滤纸.
(3)“操作1”是加热(升温);通过“操作1”再过滤,因为氢氧化钙的溶解度随温度的升高而减小,得到的白色固体的化学式为:Ca(OH)2;
(4)“吸收”中发生的化学反应是二氧化碳与氢氧化钡反应生成碳酸钡白色沉淀和水,方程式为:Ba(OH)2 + CO2 = BaCO3↓+ H2O。

 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案 小天才课时作业系列答案
小天才课时作业系列答案【题目】下列有关事实的结论合理的是( )
事实 | 结论 | |
A | Al 制品的耐腐蚀性比 Cu 制品强 | Al 的活泼性弱于铜 |
B | 金刚石和C60 均是由碳元素组成的单质 | 金刚石和C60 属于同一种物质 |
C | 在“测定空气中氧气含量”的实验中,集气瓶内水面上升约 | 氧气约占空气总质量的 |
D | H2O 和CO2 都不能使紫色石蕊变红,但把它们混合在一起时却能够使石蕊变红 | CO2 与H2O 发生了化学反应 |
A.AB.BC.CD.D