题目内容
某化工厂排出的废液中含有AgNO3和Cu(NO3)2,为了减少污染,并回收、分离金属银和铜,设计方案如图:

试写出(1)、(2)、(3)步的化学反应方程式:(1) (2) ;(3) .

试写出(1)、(2)、(3)步的化学反应方程式:(1)
考点:金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:根据在金属活动性顺序中,氢前的金属能与酸发生置换反应生成氢气,位置在前的金属能把位于其后的金属从其盐溶液中置换出来等知识进行分析.
解答:解:在金属活动性顺序中,氢前的金属能与酸发生置换反应生成氢气,位置在前的金属能把位于其后的金属从其盐溶液中置换出来,通过分析可知,铜比银活泼,铜会与硝酸银反应,铁比铜活泼,铁会与硝酸铜反应,铁会与酸反应,铜不会与酸反应,所以(1)步中的反应是铜和硝酸银反应生成硝酸铜和银,化学方程式为:Cu+2AgNO3=Cu(NO3)2+2Ag;
(2)步中的反应是铁和硝酸铜反应生成硝酸亚铁和铜,化学方程式为:Fe+Cu(NO3)2=Fe(NO3)2+Cu;
(3)步中的反应是铁和硫酸反应生成硫酸亚铁和氢气,化学方程式为:Fe+H2SO4=FeSO4+H2↑.
故答案为:Cu+2AgNO3=Cu(NO3)2+2Ag,Fe+Cu(NO3)2=Fe(NO3)2+Cu,Fe+H2SO4=FeSO4+H2↑.
(2)步中的反应是铁和硝酸铜反应生成硝酸亚铁和铜,化学方程式为:Fe+Cu(NO3)2=Fe(NO3)2+Cu;
(3)步中的反应是铁和硫酸反应生成硫酸亚铁和氢气,化学方程式为:Fe+H2SO4=FeSO4+H2↑.
故答案为:Cu+2AgNO3=Cu(NO3)2+2Ag,Fe+Cu(NO3)2=Fe(NO3)2+Cu,Fe+H2SO4=FeSO4+H2↑.
点评:本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
下列说法错误的是( )
| A、为了人体健康,应禁止使用食品添加剂 |
| B、为了防止水污染,应将工业废水处理达标后排放 |
| C、为了减少PM2.5造成的雾霾天气,应控制燃放烟花爆竹 |
| D、为了保护环境和充分利用资源,应将废旧金属回收利用 |

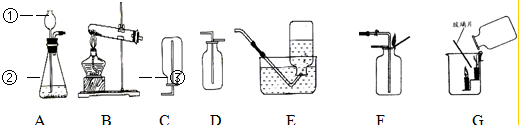
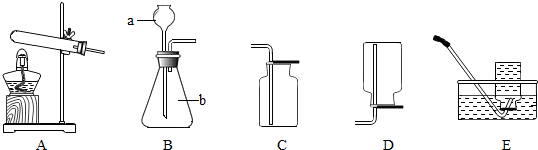
 如图所示的装置测定空气中氧气的含量.将燃烧匙中的红磷点燃迅速伸入集气瓶中并塞上橡胶塞.
如图所示的装置测定空气中氧气的含量.将燃烧匙中的红磷点燃迅速伸入集气瓶中并塞上橡胶塞.