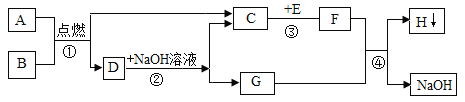
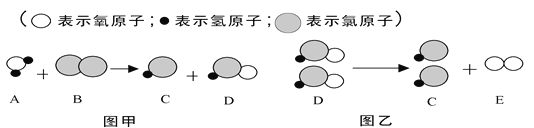
题目内容
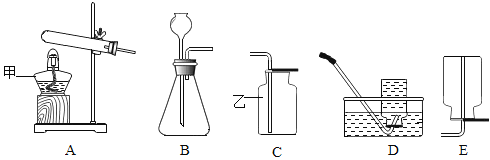
【题目】正确选择实验仪器是实验成功的重要保证,下面是实验室中常见的仪器,请按要求填空
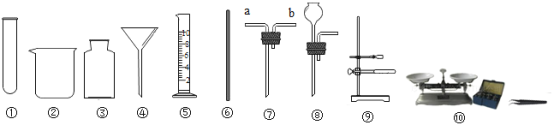
(1)配制一定溶质质量分数的氯化钠溶液,需用到的仪器有_______(填序号),还缺少的两种仪器是_______、_______(填名称);过滤粗盐水所用到的仪器有________(填序号)。
(2)实验室用石灰石和稀盐酸制取二氧化碳,可选上述仪器中的③和_______(填序号)组合成 发生装置,发生反应的化学方程式为_________。
(3)将仪器③与⑦组合,若用来排水法收集氧气,气体应从仪器⑦的__________(填“a”或“b”)端 通入,该装置还有其他的用途,请你任举一例:_________。请写出实验室加热高锰酸钾制氧气的化 学方程式__________。
【答案】②⑤⑥⑩ 药匙 胶头滴管 ②④⑥⑨ ⑧ CaCO3+2HCl═CaCl2+H2O+CO2↑ b 气体除杂或观察气体生成快慢 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
【解析】
(1)配制一定溶质质量分数的氯化钠溶液需要用到的仪器有:烧杯、量筒、玻璃棒、天平、药匙、胶头滴管。配制一定溶质质量分数的氯化钠溶液,需用到的仪器有②⑤⑥⑩,还缺少的两种仪器是药匙、胶头滴管;过滤粗盐水所用到的仪器有:烧杯、漏斗、玻璃棒、铁架台,故填写②④⑥⑨;
(2)实验室制取CO2,是在常温下,固体与液体反应,不需要加热,可选上述仪器中的③和⑧,组合成 发生装置;用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,发生反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)利用仪器③与⑦可组成一个贮气装置,收集氧气(氧气不易溶于水、密度小于水的密度)时,气体应从仪器⑦的b(短)管进入;该装置还有其他的用途,如:气体除杂或观察气体生成快慢等;实验室加热高锰酸钾制氧气的化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某兴趣小组同学对实验室制取氧气的条件进行如下探究实验.
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
I.将3.0gKClO3与1.0gMnO2均匀混合加热
II.将xgKClO3与1.0gCuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
①II中x的值为_____.
②若要证明CuO能作为KClO3分解的催化剂,则还要证明在化学反应前后CuO的____和_______都不改变.
(2)乙探究了影响双氧水分解速度的某种因素,实验数据记录如表:
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2的体积 | |
I | 50.0g | 1% | 0.1g | 9mL |
II | 50.0g | 2% | 0.1g | 16mL |
III | 50.0g | 4% | 0.1g | 31mL |
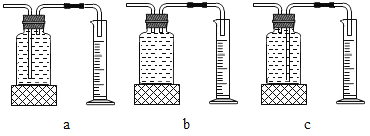
①若用上述装置测生成氧气的体积,则用图___(填“a”“b”或“c”)
②实验结论:在相同条件下,______________,双氧水分解得快.
【题目】实验室中分别用高锰酸钾、过氧化氢、氯酸钾制取比较纯净的氧气。请你按照要求回答问题:
(1)结合如图所提供装置完成下列表格。
反应物填写内容 | 反应的文字表达式 | 气体制取装置组合(填序号) |
过氧化氢(二氧化锰) | 过氧化氢 | ____________________ |
高锰酸钾 | ___________________________ | ______________________ |
氯酸钾(二氧化锰) | ___________________________ | ___________________ |
(2)请结合如图回答问题:
①写出甲、乙所指仪器名称:甲__________;乙____________;
②用过氧化氢制氧气的装置与其它两种方法的装置相比具有的优点是_____(写出1条);
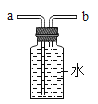
③若用如图装置收集一瓶氧气,气体应从___________ (填“a”或“b”)端进入集气瓶。
(3)小柯为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,并使用传感器测定收集到的氧气浓度,数据见表。
收集方法 | 向上排空气法 | 排水法 | ||||
氧气浓度% | 79.6 | 79.7 | 79.9 | 90.0 | 89.9 | 89.3 |
氧气平均浓度% | 79.7 | 89.7 | ||||
①小柯用向上排空气法收集氧气时,以能使放置在集气瓶瓶口的带火星木条复燃为氧气集满的标准;用排水法收集氧气时,以观察到______为氧气集满的标准。
②以上两种方法中,______法收集到的氧气更纯净。