题目内容
【题目】如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答: 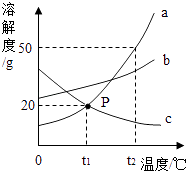
(1)t1℃时30ga物质加入到50g水中不断搅拌,能形成80g溶液吗?(填写“能”或“不能”).
(2)t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是(填写物质序号).
(3)将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是(填序号).
A.c>a=b
B.a=b>c
C.a>b>c
D.b>a>c.
【答案】
(1)不能
(2)c<b<a
(3)D
【解析】解:(1)t1℃时a物质的溶解度20g,所以t1℃时30g的a物质加入到50g水中不断搅拌,只能溶解10ga物质,所以形成溶液的质量为60g;故填:不能;(2)由溶解度曲线可知t2℃时,a、b、c三种物质的溶解度按由小到大的顺序排列是c<b<a.故填:c<b<a;(3)将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,因为a、b都不析出固体,只有c析出固体,所以三种溶液的溶质质量分数大小关系是b>a>c,;所以答案是:b>a>c.故填:D.
【考点精析】掌握固体溶解度曲线及其作用和溶质的质量分数、溶解性和溶解度的关系是解答本题的根本,需要知道1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和);溶质质量分数 =溶质质量/溶液质量*100% ;溶解度=溶质质量/溶剂质量*100g (必须选取饱和溶液);溶液质量=溶质质量(克)+溶剂质量(克) ;对于饱和溶液,溶液质量分数w = S/(S+100);所以溶解度S = 100/(1/w-1).

【题目】探究影响化学反应速率的因素
(1)发现和提出问题
镁在空气中能够剧烈燃烧,铁丝在氧气中能够剧烈燃烧,而真金不怕火炼,这说明决定物质之间能否发生反应以及反应速率的内因是 .
蜡烛在氧气中燃烧比在空气中燃烧剧烈,这一事例中影响化学反应速率的因素是;夏天,将食品放在冰箱里不容易变质,这一事例说明温度也能影响化学反应速率,温度如何影响反应速率呢?
(2)猜想与假设
温度越高,反应速率越快
收集证据
实验药品:颗粒大小相同的锌粒;两份相同溶质质量分数.不同温度的稀硫酸(20℃、40℃)
供选仪器:药匙、气体发生装置2套(气密性良好)、量筒2支、分液漏斗、秒表、胶头滴管、水槽、大试管2支.利用上述仪器和药品,补充完成下表的实验报告.
观察或测量的量 | 选用的仪器 | 实验步骤 | 实验现象 | 实验结论 |
产生相同体积(一试管)的气体所需时间 | 气体发生装置、秒表、胶头滴管、水槽、大试管、 | 温度越高,反应速率越快.反应的化学方程式是 |
该实验可以观察或测量的量有多种,除了上述观测点外,可以观察或测量的量还有(写一条) .
(3)结论与解释
从微观的角度分析“温度越高,反应速率越快”的原因是 .
(4)拓展分析
根据其他测定方位,实验小组的同学绘制了锌粒与稀硫酸反应产生氢气的速率随时间变化的曲线,如图所示,请据图分析:时间0﹣t内,反应速率逐渐加快的主要原因是 , 时间t以后,反应速率逐渐减慢的主要原因是 . 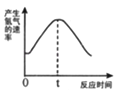
【题目】甲同学为了区别氢氧化钠和氢氧化钙溶液,设计了如图所示的四组实验方案. 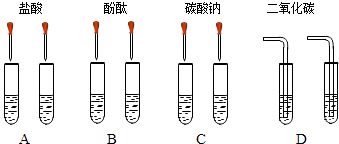
(1)其中能达到实验目的是
(2)在C组实验中发生的化学方程式为
(3)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,该现象说明有物质生成(填化学式),滴入酚酞后溶液呈红色.
(4)滴入酚酞后溶液呈红色,说明溶液呈碱性.使溶液呈碱性的物质是什么呢?甲同学进一步推测:溶液中呈碱性的物质可能是碳酸钠、氢氧化钙和三种物质中的一种,或是三种物质两两混合组成的混合物.
(5)为了验证推测,甲同学查阅资料,获悉氯化钡溶液呈中性,并设计如下实验加以验证.请根据要求完成下列空白:
实验内容 | 预测现象 | 结论 |
取少量容器中的上层溶液于试管中,加入过量的氯化钡溶液,静置 | ①若有白色沉淀,溶液呈无色 | 物质是碳酸钠 |
②若无沉淀生成,溶液呈红色 | 物质是氢氧化钙 | |
③若有白色沉淀,溶液呈红色 |
(6)乙同学认为甲同学第②步验证的结论不严密,原因是 .