题目内容
34、图(1)是小明同学设计的两个实验室制取氢气的装置.
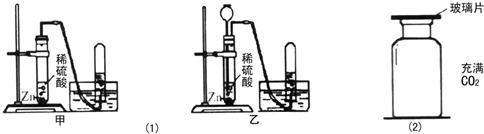
(1)与甲装置相比,乙装置的优点是
(2)用上述装置和药品制取氢气,发生反应的化学方程式为:
①导管口一有气泡就马上收集;②装置漏气;③收集气体的试管内未装满水.
(3)若将上述装置的收集方法改为
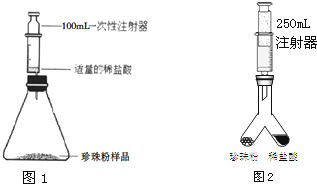
(4)如何用水和图(2)装置来验证二氧化碳能溶于水(简述操作方法):

(1)与甲装置相比,乙装置的优点是
随时补充酸溶液
.(2)用上述装置和药品制取氢气,发生反应的化学方程式为:
Zn+H2SO4=ZnSO4+H2↑
,若收集的氢气不纯,可能的原因是
①②③
(填序号).①导管口一有气泡就马上收集;②装置漏气;③收集气体的试管内未装满水.
(3)若将上述装置的收集方法改为
向上排空气
后,还可用于实验室制取二氧化碳气体,写出实验室制取该气体的化学方程式
CaCO3+2HCl=CaCl2+CO2↑+H2O
.(4)如何用水和图(2)装置来验证二氧化碳能溶于水(简述操作方法):
迅速滴入几滴水,立即盖好玻璃片震荡后,将瓶倒拿,看到玻璃片不会掉下
.分析:乙装置中有长颈漏斗,可以随时补充酸溶液;如果导管口一有气泡就马上收集、装置漏气、收集气体的试管内未装满水,这些都能导致制取的氢气中混有空气;注意二氧化碳的密度不空气大,用向上排空气法收集;用装置(2)来验证二氧化碳能溶于:迅速滴入几滴水,立即盖好玻璃片震荡后,将瓶倒拿,二氧化碳溶于水,瓶内的压力减小,在大气压的作用下,看到玻璃片不会掉下.
解答:解:(1)乙装置中有长颈漏斗,可以随时补充酸溶液;(2)制取氢体的方程式为:Zn+H2SO4=ZnSO4+H2↑; 导致氢气不纯的原因很多:①导管口一有气泡就马上收集;②装置漏气;③收集气体的试管内未装满水,这些都能导致制取的氢气中混有空气;(3)二氧化碳的密度比空气的大,用向上排空气法收集;(4)用装置(2)来验证二氧化碳能溶于水的操作方法:迅速滴入几滴水,立即盖好玻璃片震荡后,将瓶倒拿,看到玻璃片不会掉下即可.
故答案为:(1)随时补充酸溶液(2)Zn+H2SO4=ZnSO4+H2↑; ①②③
(3)向上排空气; CaCO3+2HCl=CaCl2+CO2↑+H2O (4)迅速滴入几滴水,立即盖好玻璃片震荡后,将瓶倒拿,看到玻璃片不会掉下
故答案为:(1)随时补充酸溶液(2)Zn+H2SO4=ZnSO4+H2↑; ①②③
(3)向上排空气; CaCO3+2HCl=CaCl2+CO2↑+H2O (4)迅速滴入几滴水,立即盖好玻璃片震荡后,将瓶倒拿,看到玻璃片不会掉下
点评:实验室制取氢气用到长颈漏斗,可以通过长颈漏斗随时补充酸液,明确导致氢气不纯的原因.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案
相关题目
(1)如图所示为用加热后的玻璃棒点燃白磷,来测定白磷燃烧前后质量的变化情况,用来验证质量守恒定律的实验.
①白磷在锥形瓶中燃烧时,常常导致瓶塞被冲开,实验失败.导致瓶塞被冲开的原因是什么?
②为了防止瓶塞被冲开,你能将实验作如何的改进?
③实验时,用加热后的玻璃棒点燃白磷,你还能找出其他方法点燃瓶内的白磷吗?
(2)已知工业上用电解氧化铝的方法制取单质铝的化学方程式为:2Al2O3 4Al+3O2↑对于解答:“电解10t氧化铝最多可生产多少吨铝?”一题,
4Al+3O2↑对于解答:“电解10t氧化铝最多可生产多少吨铝?”一题,
小倩和小明两位同学分别采用下面两种不同解法:
请回答下列问题:
①你认为他们的解题思路和方法都正确吗?并说明理由.
②对“34g过氧化氢完全分解产生氧气质量为多少克?”一题,你认为也能用上述两种方法解答吗?并说明理由.
③请你把②的正确解法写出来.
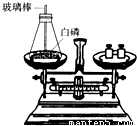
①白磷在锥形瓶中燃烧时,常常导致瓶塞被冲开,实验失败.导致瓶塞被冲开的原因是什么?
②为了防止瓶塞被冲开,你能将实验作如何的改进?
③实验时,用加热后的玻璃棒点燃白磷,你还能找出其他方法点燃瓶内的白磷吗?
(2)已知工业上用电解氧化铝的方法制取单质铝的化学方程式为:2Al2O3
 4Al+3O2↑对于解答:“电解10t氧化铝最多可生产多少吨铝?”一题,
4Al+3O2↑对于解答:“电解10t氧化铝最多可生产多少吨铝?”一题,小倩和小明两位同学分别采用下面两种不同解法:
| 小倩同学的解法 | 小明同学的解法 |
| 解:设生成的铝质量为X 2Al2O3  4Al+3O2↑ 4Al+3O2↑204108 10t X 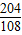 = =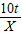 X=5.3t 答:最多可生产5.3t铝 | 解:氧化铝中铝元素的质量分数为 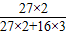 ×100%=53% ×100%=53%铝的质量为10t×53%=5.3t 答:最多可生产5.3t铝 |
①你认为他们的解题思路和方法都正确吗?并说明理由.
②对“34g过氧化氢完全分解产生氧气质量为多少克?”一题,你认为也能用上述两种方法解答吗?并说明理由.
③请你把②的正确解法写出来.

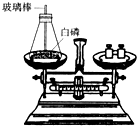 (1)如图所示为用加热后的玻璃棒点燃白磷,来测定白磷燃烧前后质量的变化情况,用来验证质量守恒定律的实验.
(1)如图所示为用加热后的玻璃棒点燃白磷,来测定白磷燃烧前后质量的变化情况,用来验证质量守恒定律的实验.