题目内容
22.(2010?湛江)某学校化学兴趣小组用NaCl固体(含有的杂质CaO)来配制一定质量分数的NaCl溶液,实验的流程图如下: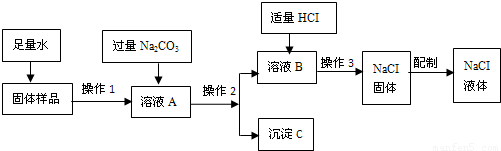
请回答:
(1)写出适量HCl加入到溶液B中所发生反应的化学方程式为.
(2)操作2的名称是,在溶液A中加入过量碳酸钠的目的是.
(3)若要配制100g质量分数为10%的氯化钠溶液,除了用到天平、烧杯、量筒外,还需用到的玻璃仪器是,其作用是.
【答案】分析:(1)根据碳酸钠与盐酸反应的原理分析;
(2)根据过滤操作的适用范围分析,根据除杂时所加试剂的原则分析;
(3)根据玻璃棒的作用分析;
解答:解:(1)Na2CO3会与盐酸反应,故答案为:Na2CO3+2HCl═2NaCl+H2O+CO2↑
(2)把碳酸钠加入A溶液中后,生成碳酸钙沉淀和氯化钠溶液,要把碳酸钙除去,可以用过滤的方法,所加碳酸钠一定要足量,以便把A中的氢氧化钙除完.
故答案为:过滤 充分除尽溶液中的氢氧化钙
(3)配制一定质量分数的溶液用到的仪器有:天平、烧杯、量筒、玻璃棒.
故答案为:玻璃棒 搅拌加快溶解
点评:该题目是根据实验流程图来分析问题,所以做这类题的关键是理清实验流程图.除某溶液中的杂质时所加除杂试剂一定要过量,以便把溶液中的杂质除完,但最后还需要把所加试剂也要除完,不能引入新的杂质.
(2)根据过滤操作的适用范围分析,根据除杂时所加试剂的原则分析;
(3)根据玻璃棒的作用分析;
解答:解:(1)Na2CO3会与盐酸反应,故答案为:Na2CO3+2HCl═2NaCl+H2O+CO2↑
(2)把碳酸钠加入A溶液中后,生成碳酸钙沉淀和氯化钠溶液,要把碳酸钙除去,可以用过滤的方法,所加碳酸钠一定要足量,以便把A中的氢氧化钙除完.
故答案为:过滤 充分除尽溶液中的氢氧化钙
(3)配制一定质量分数的溶液用到的仪器有:天平、烧杯、量筒、玻璃棒.
故答案为:玻璃棒 搅拌加快溶解
点评:该题目是根据实验流程图来分析问题,所以做这类题的关键是理清实验流程图.除某溶液中的杂质时所加除杂试剂一定要过量,以便把溶液中的杂质除完,但最后还需要把所加试剂也要除完,不能引入新的杂质.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
25.(2010?湛江)我市某校初三(1)班学生去湖光岩春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来讲行实验测定,(样品中的杂质不溶于水,且不与盐酸反应),测得数据如下表:
试问答:
(1)10.0g样品与45g盐酸充分反应后,盐酸是否还剩余______(填“是”或“否”),样品中碳酸钙的质量分数是______.
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳多少克?(写出计算过程,计算结果精确到小数点后两位)
| 甲同学 | 乙同学 | 丙同学 | 丁同学 | |
| 所取石灰石样品质量(g) | 10.0 | 10.0 | 10.0 | 10.0 |
| 加入盐酸的质量(g) | 20.0 | 30.0 | 45.0 | 50.0 |
| 剩余固体的质量(g) | 6.0 | 4.0 | 1.0 | 1.0 |
(1)10.0g样品与45g盐酸充分反应后,盐酸是否还剩余______(填“是”或“否”),样品中碳酸钙的质量分数是______.
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳多少克?(写出计算过程,计算结果精确到小数点后两位)