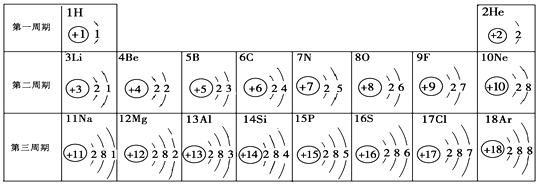
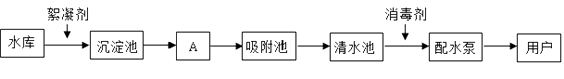
题目内容
【题目】金属单质M与非金属单质硫发生如下反应为2M + S ![]() M2S。甲、乙二组学生在实验室分别进行该实验,加入的M和硫的质量各不相同。充分反应后,实验数据记录如下表,则M的相对原子质量是( )
M2S。甲、乙二组学生在实验室分别进行该实验,加入的M和硫的质量各不相同。充分反应后,实验数据记录如下表,则M的相对原子质量是( )
M的质量/ g | S的质量/ g | M2S的质量/ g | |
甲 | 6.0 | 2.5 | 7.5 |
乙 | 7.0 | 1.5 | 7.5 |
A.64
B.56
C.39
D.23
【答案】A
【解析】从题中的数据可知,甲中硫过量,乙中M过量,6.0gM能与1.5g硫完全反应,
2M + | S |
2M | 32 |
6g | 1.5g |
![]() 2M:32=6g:1.5g
2M:32=6g:1.5g
得到M=64,故答案选择A
根据甲、乙两同学实验数据,结合题设中“充分反应时,所用A和硫的质量各不相同,但总质量相等,都是7.5g”,可知,甲、乙组中的物质都没有完全反应,因为反应前物质的质量之和大于反应后生成的物质,甲中硫过量,乙中M过量分析,可知反应2M+S═M2S,判断恰好完全反应时A、S用量比;利用所判断的恰好完全反应时M、S用量比,求出M的相对原子质量;

练习册系列答案
相关题目
【题目】将4.0gCu – Zn合金粉末放到盛有10g稀硫酸的烧杯中,恰好完全反应,Cu不与硫酸反应。相关实验数据如下:
反应前物质的质量 / g | 反应后物质的质量 / g | |
Cu – Zn合金 | 稀硫酸 | 烧杯中物质 |
4.0 | 10 | 13.96 |
(1)生成氢气的质量是;
(2)若不考虑该合金中除Cu、Zn以外的其他成分,请计算原Cu – Zn合金中Zn的质量为。写出必要的计算过程。