题目内容
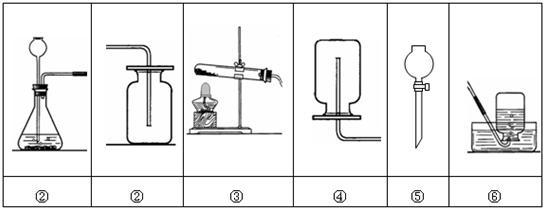
(2011?淄博)化学实验是学习化学和进行科学研究的重要方法和途径.学会气体物质的制备方法是研究气体、利用气体的基础.请根据下图回答有关问题:
(1)在常温下实验室欲制取氧气所选用的装置是______(填序号),为了便于调控反应的进行,可以对发生装置进行改进,请简要说明你的改进措施______.
(2)从上述仪器中选择一种你比较熟悉的仪器,写出它的名称______,简要写出它的用途______.
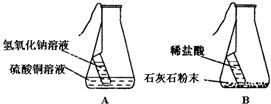
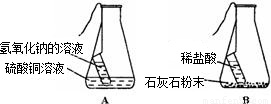
(3)同学们以“化学反应中,反应物与生成物的质量关系”为课题进行探究.经讨论分析、查阅资料后设计了A、B两套实验装置,并在实验过程中做到操作规范、准确称量和细致观察.实验完毕后,使用A装置进行实验得到的结果是:反应前后反应物的总质量与生成物的总质量相等;而使用B装置进行实验得到的结果是:反应前后反应物的总质量与生成物的总质量不相等.请你分析导致出现两种不同结果的原因是______.
写出B装置中发生反应的化学方程式______.
【答案】分析:(1)熟记实验室制取氧气的两种装置,并根据题目的要求做出选择;
(2)试管是我们最熟悉的仪器,我们可以选择试管,并说明其作用;
(3)从A装置中无气体生成,B装置中有气体生成考虑;熟记稀盐酸与石灰石反应的化学反应式.
解答:解:(1)根据题目可知,能改进的制取氧气的装置是①,可以把①中的长颈漏斗改成分液漏斗,控制反应式的速率;因二氧化碳密度大于空气的密度,并且不易溶于水,可选用②或⑥收集氧气.
故答案为:①②或①⑥;用⑤分液漏斗代替长颈漏斗;
(2)实验室常见仪器是试管,它可作为少量物质的反应容器.
故答案为:试管;作为少量物质的反应容器;
(3)A中氢氧化钠溶液与硫酸铜溶液反应,氢氧化铜沉淀和硫酸钠,所有物质都没有脱离体系;而B中稀盐酸与石灰石粉末反应有二氧化碳气体生成,二氧化碳散失到空气中,使剩余物质的质量比原物质质量减小.稀盐酸与石灰石粉末反应式的化学式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.
故答案为:A中的两种物质反应产生了沉淀没有脱离体系,所以质量不变,而B中产生了CO2散失,使剩余物质的质量比原物质质量减小;CaCO3+2HCl=CaCl2+H2O+CO2↑.
点评:发生装置的选择要考虑反应物的状态和反应条件,分液漏斗可以控制反应的速率等,这些是化学实验中的常见问题,同学们一定要记清.
(2)试管是我们最熟悉的仪器,我们可以选择试管,并说明其作用;
(3)从A装置中无气体生成,B装置中有气体生成考虑;熟记稀盐酸与石灰石反应的化学反应式.
解答:解:(1)根据题目可知,能改进的制取氧气的装置是①,可以把①中的长颈漏斗改成分液漏斗,控制反应式的速率;因二氧化碳密度大于空气的密度,并且不易溶于水,可选用②或⑥收集氧气.
故答案为:①②或①⑥;用⑤分液漏斗代替长颈漏斗;
(2)实验室常见仪器是试管,它可作为少量物质的反应容器.
故答案为:试管;作为少量物质的反应容器;
(3)A中氢氧化钠溶液与硫酸铜溶液反应,氢氧化铜沉淀和硫酸钠,所有物质都没有脱离体系;而B中稀盐酸与石灰石粉末反应有二氧化碳气体生成,二氧化碳散失到空气中,使剩余物质的质量比原物质质量减小.稀盐酸与石灰石粉末反应式的化学式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.
故答案为:A中的两种物质反应产生了沉淀没有脱离体系,所以质量不变,而B中产生了CO2散失,使剩余物质的质量比原物质质量减小;CaCO3+2HCl=CaCl2+H2O+CO2↑.
点评:发生装置的选择要考虑反应物的状态和反应条件,分液漏斗可以控制反应的速率等,这些是化学实验中的常见问题,同学们一定要记清.

练习册系列答案
相关题目
(2011?淄博)化学是在原子、分子的水平上对物质进行研究的基础自然学科.请你运用分子的性质判断,以下事实的解释错误的是( )
| 序号 | 事实 | 解释 |
| A | 新装修的房间中有异味 | 分子是不断运动的 |
| B | 用扫描隧道显微镜观测到原子和分子 | 分子的体积很小 |
| C | 用乙烯合成聚乙烯塑料 | 分子之间有间隔 |
| D | 过氧化氢分解生成水和氧气 | 分子可以再分 |