题目内容
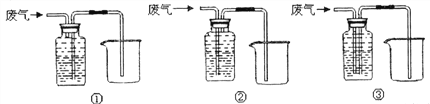
【题目】下表是NaCl、KClO3在不同温度下的溶解度(单位:g/100g水)。
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
S(NaCl) | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
S(KClO3) | 3.3 | 7.3 | 13.9 | 23.8 | 37.5 | 56.3 |
20℃时,NaCl的溶解度为_______ g/100g水;
40℃时,将10gKClO3放入100g水中充分溶解,所得溶液溶质质量分数为_______(最简分数);
③ “海水晒盐”利用的方法是_______(填“蒸发结晶”或“降温结晶”);
④ 工业上用氯化钠溶液制备氯酸钾,主要流程如下:
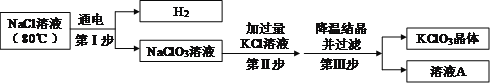
(第Ⅱ步中发生的反应:NaClO3+KCl→NaCl+KClO3)
上述流程中,氯化钠溶液中的水是否参与第Ⅰ步化学反应?_______(填“是”或“否”)。
溶液A中的溶质除NaCl外,还含有_______(填化学式)。
【答案】36.01/11蒸发结晶是KCl、KClO3
【解析】(1)溶解度是一定温度下,100g溶剂里达到饱和时,所溶解的溶质的质量。由题中信息可知20℃时,NaCl的溶解度为36.0 g/100g水;(2). 40℃时,硝酸钾的溶解度为13.9g,将10gKClO3放入100g水中能完全溶解,所得溶液溶质质量分数为10g ÷(10g+100g)×100%=1/11 (3). 氯化钠的溶解度受温度的影响比较小,所以应该用蒸发结晶的方法式食盐从溶液中分离出来 (4).氯化钠和水 在通电条件下生成氢氧化钠、氯气、氢气(5). 因步骤Ⅱ中加入过量的氯化钾,所以溶液A中有氯化钠、KCl、KClO3

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目