题目内容
【题目】现有家庭食用碱样品12 g(主要成分Na2CO3其他成分不与酸反应),向其中加入某未知浓度的盐酸,生成气体的质量与加入盐酸的质量关系如下图。请计算:(方程式:Na2CO3+2HCl=2NaCl+H2O+CO2 ↑,写出计算过程,结果精确到0.1%)
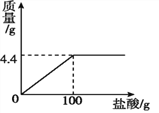
(1) 12g食用碱样品中碳酸钠的质量是多少?
(2)所加盐酸的溶质的质量分数是多少?
【答案】(1)10.6g; (2) 7.3%
【解析】解: 设12 g食用碱样品中碳酸钠的质量是x ,所加盐酸的溶质的质量为y
Na2CO3+2HCl=2NaCl+2H2O+CO2 ↑
106 73 44
x y 4.4g
![]() =
=![]() ,x=10.6g
,x=10.6g
![]() =
=![]() ,y =7.3g
,y =7.3g
﹙1﹚12 g食用碱样品中碳酸钠的质量是10.6g
﹙2﹚所加盐酸的溶质的质量分数为∶![]() ×100%=7.3%
×100%=7.3%
答:﹙1﹚2 g食用碱样品中碳酸钠的质量是10.6g ;﹙2﹚所加盐酸的溶质的质量分数为7.3%
点睛∶根据化学方程式进行计算,首先要求化学方程式书写必须正确。

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
【题目】下列实验方法一定能达到实验目的的是(______)
选项 | 实验目的 | 实验方法 |
A | 检验一瓶气体是否为 | 将燃着的木条伸入瓶中 |
B | 鉴别 | 分别点燃,在火焰上方罩一干冷烧杯 |
C | 鉴别硬水和软水 | 加入适量的肥皂水 |
D | 比较Zn、Cu、Ag的金属活动性 |
A.A B.B C.C D.____________