��Ŀ����
��ش��������⣺
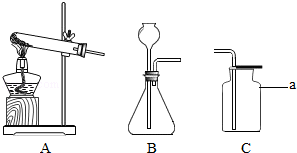
��ͼ1��ʵ�������ü�������غͶ������̵Ļ������ȡ�����ķ���װ�ã���ָ��ͼ���������ԵĴ����� �������� ����
ij��ѧС���ͬѧ�������ϵ�֪����������KO2��һ�ֹ��壬�����������̼��Ӧ����������4KO2+2CO2=2K2CO2+3O2�����⣬�������ػ�����ˮ���Ȼ�淋����ʷ�����Ӧ����С��ͬѧ�����ô���ʯ��ϡ���ᷴӦ���ɵĶ�����̼�볬�����ط�Ӧ����ȡ������ʵ����ʹ������ͼ2װ�ã�
��ش��������⣺
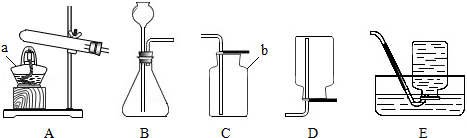
��Ϊ���������ʵ�飬��װ�õ�����˳��Ϊ�� ��������ţ���
��װ��D���������� ����
��װ��E���������� ����
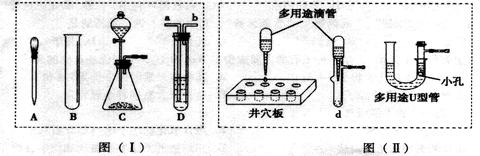
��������ͼ3װ���ռ��Ƶõ�������������Ӧ���� ���ˣ���a��b�����룮
�Թܿ�������б�������������Թܿڹ�����BECADF������δ�μӷ�Ӧ�Ķ�����̼����ȥCO2�л��е�HCl���壻b��
�������������ʵ�������ü�������غͶ������̵Ļ������ȡ����ʱΪ��ֹ����ˮ�ĵ����Թܿ�Ҫ��������б��Ϊ����������ų��������ܲ������뵼���ܹ�������ͼ���������ԵĴ����Թܿ�������б���ڵ����������Թܿڹ�����
�ô���ʯ��ϡ���ᷴӦ���ɵĶ�����̼�ķ���װ����B����Ϊ������������ˮ���Ȼ�������ʷ�����Ӧ����������лӷ��ԣ�����Ҫͨ��̼��������Һ���ջӷ��������Ȼ������壻��ͨ������������ˮ��Ȼ������Ķ�����̼�볬�����ط�Ӧ��Ϊ�ռ�����������������Ҫ�ѹ����Ķ�����̼��ȥ��ͨ��̼������Һ���������ռ���������ӵ�˳���ǣ�BECADF��
����װ��D�������ǣ�����δ�μӷ�Ӧ�Ķ�����̼�����ռ���������������װ��E�������ǣ���ȥCO2�л��е�HCl���壬��ֹ�����������Ȼ��ⷴӦ��
��Ϊ�������ܶȱȿ����ʻ�ۼ����·����������Ƕ̹ܩ�b��
���㣺��������ķ���װ�ú��ռ�װ����ѡȡ����������ľ��������ӣ���
���������⿼����������ȡ�ij���װ�õ���������������Ŀ����Ϣ���е�������ȡ���ռ��ȣ�Ҫ�������ն�����̼�����������ʣ�ͬʱ�ڳ�ȥһ�������е���������ʱ��Ҫ������Ŀ����Ϣ�����������ʽ���ѡ��Ҫ�����ʳ�ȥ���ֲ���Ӱ�챻�����ʵ����塣

 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�����һ���ж������ʵ���ɫ��Һ�����ڸ���Һ���������ʣ������¼��ֲ²⣬���к�������
| A��H2SO4��KOH��NaCl | B��NaNO3��NaCl��CuCl2 |
| C��AgNO3��NaCl��HCl | D��H2SO4��Na2SO4��KNO3 |
�������и������ʣ������Լ����������������ǣ�������
| ѡ�� | �����ֵ����� | ���� |
| A | �ϳ���ά�ʹ���ë | �ֱ�ȡ�������գ�������ζ |
| B | CaCl2��Һ��NaCl��Һ | �ֱ�ȡ������Һ������������Һ���۲����� |
| C | �ƾ���ˮ | ����ζ |
| D | ̼�ۺ�����ͭ | �ֱ�ȡ��������ϡ���ᣬ�۲����� |
�±��У���ȥ���������������ʵķ����ͷ�Ӧ���������ȷ����
| ѡ�� | ���� | �������� | ��ȥ���� | ��Ӧ���� |
| A | CuO�� | Cu�� | �ڿ����м��� | ���Ϸ�Ӧ |
| B | CO2 | CO | ͨ�����ȵ�CuO | �û���Ӧ |
| C | H2 | HCl | ͨ��ʢ����������Һ��ϴ��ƿ | �ֽⷴӦ |
| D | KCl | K2SO4 | �ܽ⣬�����������ᱵ��Һ�������� | ���ֽⷴӦ |