题目内容
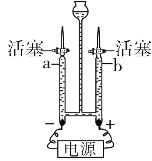
【题目】(1)电源种类---____________
(2)加入稀硫酸或氢氧化钠溶液的目的是_____________
(3)电解水的实验中,负极得到______气,正负两极气体的体积比是_________,质量比是_________,
(4)由该实验得出的结论是水是由_______组成的,水是由____ 构成的。每一个水分子是由___和______构成的。
(5)电解水的化学表达式为:__________。
【答案】直流电 增强水的导电性 氢 1:2 8:1 氢元素和氧元素 水分子 两个氢原子 一个氧原子 H2O![]() H2+O2
H2+O2
【解析】
(1)电解水的实验采用的是直流电;
(2)纯水不易导电,为增强水的导电性常加入少量稀硫酸或氢氧化钠溶液使其易导电的物质,使反应顺利进行;
(3)电解水实验中,正极产生氧气,负极产生氢气,二者的体积比是1:2,质量比是8:1;
(4)化学反应前后元素的种类不变,由电解水生成氢气和氧气可知水是由氢元素和氧元素组成的;水是由水分子构成的,每一个水分子是由两个氢原子和一个氧原子构成的;
(5)水通电生成氢气和氧气,反应的化学表达式为:H2O![]() H2+O2。
H2+O2。

【题目】空气是人类赖以生存的自然资源。请按要求回答相关问题(所涉及的物质用化学式填空):
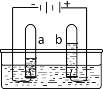
(1)氮气、氧气、氦气和二氧化碳都是空气的成分。

图中a代表的气体是________;引起温室效应的是_______;通电时发出有色光的是_______;供给呼吸的是________。
(2)空气中主要组分的沸点如下表:
组分 | 氮气 | 氧气 | 二氧化碳 |
沸点(℃) | -195.8 | -183.0 | -78.5 |
空气是工业上制取大量氧气的原料,工业制氧气属于________变化(填“物理”或“化学”)。将液态空气升温至-195℃,收集逸出的物质,此时逸出的物质主要是________;继续升温至-183℃,将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是___________。
(3)下列叙述正确的是________。
A.进入久未开启的菜窖前,应先做灯火实验
B.二氧化碳有毒,含量过高时会使人死亡
C.夏天从冰箱里拿出冰棍周围有白雾,是空气中的水蒸气液化
D.空气中各成分含量是相对稳定的
【题目】早在十七世纪,英国化学家波义耳由于实验设计“失误”,错过了发现质量守恒定律的机会,请你改进他的试验方法,以验证质量守恒定律。
波义耳的实验(1673年) | 我的改进 |
在密闭的容器中燃烧金属,得到了金属灰 | 称量密闭的容器(连同里面的金属),进行燃烧实验 |
打开容器,称量金属灰的质量 | 燃烧结束后,称量________________ |
发现比原金属质量_____________(填“增加”或“减少”或“不变”) | 发现总质量和燃烧前一样。若反应容器内的反应是镁带燃烧,其反应的化学方程式是 _____________________________________ |
启发:用实验来研究化学反应前后反应物和生成物之间的质量关系时,应该在______________ 容器中进行。 | |
拓展:应用质量守恒定律验证石墨的元素组成。 实验步骤:称量a克石墨,放在盛有足量氧气的密闭容器中引燃;反应结束后,用足量的b克澄清石灰水吸收生成的气体(吸收完全),发生的反应方程式为:____________________ 称量石灰水的质量变为c克。 根据______________________________(现象),可知石墨中含有碳元素; 根据a=_______________________(用含b、c的关系式表示),可知石墨中只含有碳元素 | |