题目内容
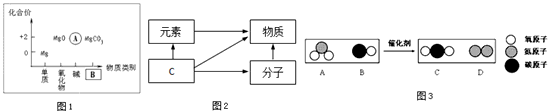
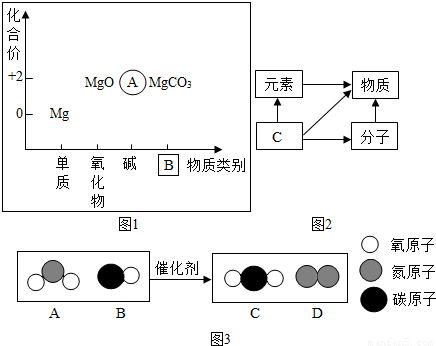
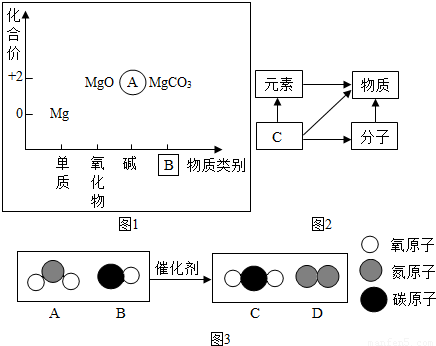
(1)以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.如图1为镁的价类图,分析该图后填写:A处的化学式为:________,B处的物质类别是:________.
(2)如图2中C是________.
(3)在铜、氯化钠、二氧化碳三种物质中,由分子构成的是________.
(4)葡萄糖酸钙【化学式为(C6H11O7)2Ca】由________种元素组成,其中碳、氢元素的质量比为________.
(5)如图3为某反应的微观示意图.
①该反应中B与D的质量比是________(结果用最简整数比表示).
②对此反应的叙述正确的是________(填序号).
a.反应前后各元素化合价均未改变 b.用同种元素可以组成不同物质
c.加入催化剂可提高产物质量 d.利用此反应可减少有毒气体的排放.
解:(1)碱为Mg(OH)2 碳酸镁属于盐.
(2)从相互关系可推断A是原子;
(3)二氧化碳是由分子构成的,铜由原子构成,氯化钠由离子构成;
(4)根据葡萄糖酸钙【化学式为(C6H11O7)2Ca】可知由四种元素组成;其中碳、氢元素的质量比为(12×6):(1×11)=72:11;
(5)①由粒子模型看出是CO和NO2反应生成N2和CO2,反应的化学方程式为:4CO+2NO2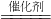 N2+4CO2
N2+4CO2
其中CO和N2的质量比是(28×4):(28)=4:1;
②a、在此反应中,有单质生成,故元素的化合价发生改变,b、反应前后元素的种类不变,但物质的种类发生改变,说明同种元素可以组成不同物质;C、加入催化剂不能提高产物质量,只能改变反应速率;d、反应物都是有毒的,生成物无毒,故利用此反应可减少有毒气体的排放.故选bd.
故答案为:
(1)Mg(OH)2、盐
(2)原子.
(3)二氧化碳.
(4)四,72:11.
(5)①4:1.②bd.
分析:(1)根据物质的分类解答
(2)根据分子、原子、离子、元素之间的关系判断;
(3)根据物质的粒子构成判断;
(4)根据葡萄糖的化学式计算;
(5)根据分子结构写出分子的化学式,然后写出化学方程式,再根据质量守恒定律计算.
点评:了解分子、原子、离子、元素之间的关系,学会利用微粒观点及模型图的应用,可帮助学生正确认识常见物质的微粒组成,树立微粒观.
(2)从相互关系可推断A是原子;
(3)二氧化碳是由分子构成的,铜由原子构成,氯化钠由离子构成;
(4)根据葡萄糖酸钙【化学式为(C6H11O7)2Ca】可知由四种元素组成;其中碳、氢元素的质量比为(12×6):(1×11)=72:11;
(5)①由粒子模型看出是CO和NO2反应生成N2和CO2,反应的化学方程式为:4CO+2NO2
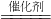 N2+4CO2
N2+4CO2其中CO和N2的质量比是(28×4):(28)=4:1;
②a、在此反应中,有单质生成,故元素的化合价发生改变,b、反应前后元素的种类不变,但物质的种类发生改变,说明同种元素可以组成不同物质;C、加入催化剂不能提高产物质量,只能改变反应速率;d、反应物都是有毒的,生成物无毒,故利用此反应可减少有毒气体的排放.故选bd.
故答案为:
(1)Mg(OH)2、盐
(2)原子.
(3)二氧化碳.
(4)四,72:11.
(5)①4:1.②bd.
分析:(1)根据物质的分类解答
(2)根据分子、原子、离子、元素之间的关系判断;
(3)根据物质的粒子构成判断;
(4)根据葡萄糖的化学式计算;
(5)根据分子结构写出分子的化学式,然后写出化学方程式,再根据质量守恒定律计算.
点评:了解分子、原子、离子、元素之间的关系,学会利用微粒观点及模型图的应用,可帮助学生正确认识常见物质的微粒组成,树立微粒观.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案
相关题目
 (2012?邗江区二模)
(2012?邗江区二模)