��Ŀ����
����Ŀ����������ȵ�X��Y��Z���ֽ���ͬʱ�����������ʵ�����������ͬ��������ϡ�����У���֪X��Y��Z���������о�Ϊ+2�ۣ�����Ӧ���������������뷴Ӧʱ��Ĺ�ϵ��ͼ1��ʾ������ͼ�����ṩ����Ϣ�ó��Ľ�����ȷ���ǣ� �� 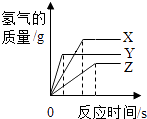
A.�ų�H2��������Z��Y��X
B.��Ӧ����������X
C.�������˳����Y��X��Z
D.���ԭ��������X��Y��Z
���𰸡�C
���������⣺A�����ݷ�Ӧ����H2�������뷴Ӧʱ��Ĺ�ϵͼ��ʾ�������ֽ�����ȫ��Ӧ�ų�H2��������X��Y��Z����A���� B�����ݷ�Ӧ����H2�������뷴Ӧʱ��Ĺ�ϵͼ��ʾ�������������ֽ���Y����ȫ��Ӧ����˷�Ӧ�ٶ�������Y����B����
C�����ݷ�Ӧ����H2�������뷴Ӧʱ��Ĺ�ϵͼ��ʾ�������ֽ������ڷ�����Ӧʱ����ͬʱ����Y�ų���������X������Z�����ж����ֽ�����Y�����ǿ����C��ȷ��
D�����ֽ����Ļ��ϼۡ���������������ȣ���ȫ��Ӧ�ų���������������������ԭ�������ɷ��ȣ�����������������ԭ������С�����ݷ�Ӧ����H2�������뷴Ӧʱ��Ĺ�ϵͼ��ʾ�������ֽ�����ȫ��Ӧ�ų�H2��������X��Y��Z����˿��ж����ԭ��������X��Y��Z����D����
��ѡ��C��
�����㾫�������ڱ��⿼��Ľ������ϵ�ѡ�����ݣ���Ҫ�˽��ɫ������ͨ��ָ�����̡��������ǵĺϽ��ؽ�������ͭ��п��Ǧ�ȣ���ɫ��������������ơ�þ�����ȣ���ɫ������ͨ����ָ����ɫ��������������������ܵó���ȷ�𰸣�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�