题目内容
【题目】以下是在实验室里制取气体时常用的部分仪器,请回答问题. 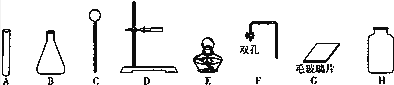
(1)标号为H的仪器名称是;
(2)实验室用大理石和稀盐酸制备二氧化碳气体,不可能选用的仪器是 , 该反应的化学方程式为:
(3)要配制150g溶质质量分数为5%的过氧化氢溶液,需要溶质质量分数为30%的过氧化氢溶液g;
(4)用配制好的5%的过氧化氢溶液136g和适量二氧化锰混合,理论上可制得氧气的质量为g.
【答案】
(1)集气瓶
(2)E;CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)25
(4)3.2
【解析】解:(1)标号为H的仪器名称是集气瓶.(2)实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,属于固液常温型,同时生成氯化钙、水,反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.(3)需溶质质量分数为30%的过氧化氢溶液的质量: ![]() =25g.
=25g.
4)解:136g×5%=6.8g.
设充分反应可制得氧气的质量为x.
2H2O2![]() 2H2O+O2↑
2H2O+O2↑
68 32
6.8g x
则 ![]() ,解得x=3.2g.
,解得x=3.2g.
答:充分反应可制得氧气3.2g.
所以答案是:(1)集气瓶;(2)E,CaCO3+2HCl=CaCl2+H2O+CO2↑:(3)25;(4)3.2.
【考点精析】掌握书写化学方程式、文字表达式、电离方程式和根据化学反应方程式的计算是解答本题的根本,需要知道注意:a、配平 b、条件 c、箭号;各物质间质量比=系数×相对分子质量之比.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目