题目内容
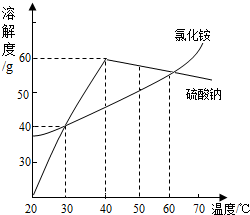
 如图为氯化铵和硫酸钠的溶解度曲线.下面说法中不正确的是( )
如图为氯化铵和硫酸钠的溶解度曲线.下面说法中不正确的是( )分析:A、30℃时氯化铵和硫酸钠的溶解度相等,据饱和溶液中溶质的质量分数=
×100%可知溶解度相等则溶质的质量分数相等;
B、一定温度下的饱和溶液中溶解度大则溶质的质量分数大;
C、据硫酸钠的溶解度随温度变化分析解答;
D、60℃降温至40℃,硫酸钠的溶解度逐渐增大,据此分析解答.
| 溶解度 |
| 溶解度+100g |
B、一定温度下的饱和溶液中溶解度大则溶质的质量分数大;
C、据硫酸钠的溶解度随温度变化分析解答;
D、60℃降温至40℃,硫酸钠的溶解度逐渐增大,据此分析解答.
解答:解:A、30℃时氯化铵和硫酸钠的溶解度相等,据饱和溶液中溶质的质量分数可知:溶解度相等则饱和溶液中溶质的质量分数相等,正确;
B、由图可知:40℃时硫酸钠的溶解度最大,所以硫酸钠饱和溶液中溶质的质量分数在该温度时最大,正确;
C、观察溶解度曲线可知:在50℃至40℃时硫酸钠的溶解度随温度降低而增大,降温不会析出晶体,再继续降温,饱和溶液才晶体,故描述错误;
D、60℃降温至40℃,硫酸钠的溶解度逐渐增大,所以在该温度内饱和溶液降温不会析出晶体,溶质不变、溶剂不变,则溶质的质量分数不变,正确;
故选C.
B、由图可知:40℃时硫酸钠的溶解度最大,所以硫酸钠饱和溶液中溶质的质量分数在该温度时最大,正确;
C、观察溶解度曲线可知:在50℃至40℃时硫酸钠的溶解度随温度降低而增大,降温不会析出晶体,再继续降温,饱和溶液才晶体,故描述错误;
D、60℃降温至40℃,硫酸钠的溶解度逐渐增大,所以在该温度内饱和溶液降温不会析出晶体,溶质不变、溶剂不变,则溶质的质量分数不变,正确;
故选C.
点评:了解溶解度曲线的意义、饱和溶液中溶质的质量分数的计算方法,并能结合物质的溶解度变化曲线灵活分析解答问题.

练习册系列答案
 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案
相关题目
“溶液”在日常生产生活中应用广泛,因而我们要掌握一些有关“物质溶解”的知识.
(1)20℃时,17gKCl溶解在50g水中恰好达到饱和,则该温度下KCl的溶解度为 g.
(2)相同条件下,氢氧化铜难溶于水,高锰酸钾易溶于水,说明固体物质的溶解能力和溶质的性质有关;请你举例说明固体物质的溶解能力还与什么因素有关?
(3)我们还发现,在用洗衣粉洗衣服时(在等量的水里放等量的洗衣粉),夏天洗衣粉很快溶解了,冬天反复搅拌后往往还会有许多洗衣粉颗粒悬浮水中,这说明洗衣粉的溶解度随着温度升高而 .当你用湿手取少量洗衣粉时,感觉手烫,你认为产生这种现象的原因是 ;若取用X固体代替洗衣粉与水混合,也得到与上述相似的现象,则加入的X固体可能是下列哪种物质 .(填下列选项前的字母)
A.氧化钙B.硝酸铵 C.氢氧化钠D.氯化钠)
(4)如图为氯化铵和硫酸钠的溶解度曲线,当把相同质量的氯化铵和硫酸钠的饱和溶液从50℃降到20℃时,析出晶体最多的是 .
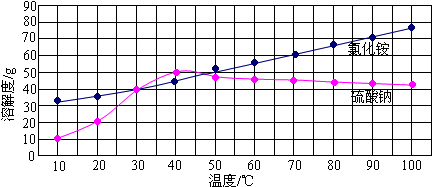
(5)在40℃时取两份100g水分别往加入50克氯化铵和50克硫酸钠,充分搅拌后,升温到60℃,下列说法正确的是 .
A.40℃时,两溶液均为饱和溶液
B.40℃时,两溶液质质量分数相等
C.50℃时.两溶液仍为饱和溶液
D.60℃时,硫酸钠溶液仍为饱和溶液,氯化铵溶液为不饱和溶液
E.60℃时,两溶液溶质质量分数相等
F.60℃时,两溶液中溶质质量分数不相等.
(1)20℃时,17gKCl溶解在50g水中恰好达到饱和,则该温度下KCl的溶解度为
(2)相同条件下,氢氧化铜难溶于水,高锰酸钾易溶于水,说明固体物质的溶解能力和溶质的性质有关;请你举例说明固体物质的溶解能力还与什么因素有关?
| 影响固体物质的溶解能力 | 举例说明 |
A.氧化钙B.硝酸铵 C.氢氧化钠D.氯化钠)
(4)如图为氯化铵和硫酸钠的溶解度曲线,当把相同质量的氯化铵和硫酸钠的饱和溶液从50℃降到20℃时,析出晶体最多的是

(5)在40℃时取两份100g水分别往加入50克氯化铵和50克硫酸钠,充分搅拌后,升温到60℃,下列说法正确的是
A.40℃时,两溶液均为饱和溶液
B.40℃时,两溶液质质量分数相等
C.50℃时.两溶液仍为饱和溶液
D.60℃时,硫酸钠溶液仍为饱和溶液,氯化铵溶液为不饱和溶液
E.60℃时,两溶液溶质质量分数相等
F.60℃时,两溶液中溶质质量分数不相等.
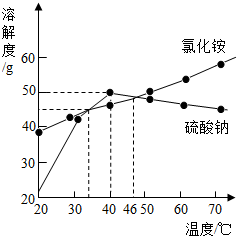 如图为氯化铵和硫酸钠的溶解度曲线.请回答:
如图为氯化铵和硫酸钠的溶解度曲线.请回答: 14、如图为氯化铵和硫酸钠的溶解度曲线,请回答下列问题:
14、如图为氯化铵和硫酸钠的溶解度曲线,请回答下列问题: