��Ŀ����
����Ŀ����7�֣�ͭ�������������õĽ���֮һ�� ұ��ͭ����ͭ��ʯ������ȸʯ������Ҫ�ɷ�Ϊ��ʽ̼��ͭ[Cu2(OH)2CO3]����ʽ̼��ͭ��һ����ɫ�IJ�����ˮ�Ĺ��壬�����ֽ⣬������Ϸ��������汸���̼���εĻ�ѧ���ʣ����������ᷢ����Ӧ��
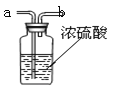
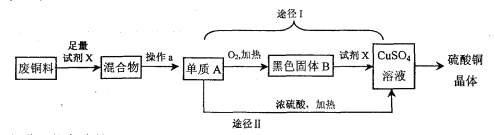
���ͬѧ����ʵ�������Լ�ʽ̼��ͭ�����ۡ�ϡ����Ϊԭ������ȡͭ�����ʵ���������£�
![]()
��ش��������⣺
��1����ʽ̼��ͭ�к��� ��Ԫ�ء�
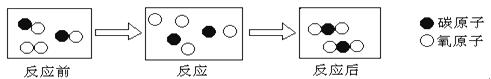
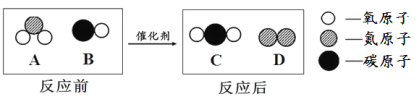
��2����ʽ̼��ͭ���ȷֽ��������ֳ����������������һ��ͨ���Ǻ�ɫ���壬��д���ú�ɫ������ľ̿������Ӧ�Ļ�ѧ����ʽ ����ʽ̼��ͭ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪCu2(OH)2CO3+4HCl====2CuCl2+CO2��+3H2O��Ԥ��ʵ������ ��
��3������ȸʯ��Ʒ�к���44.4g Cu2(OH)2CO3����ַ�Ӧ���������ܵõ�ͭ������Ϊ g��
���𰸡���(1) 4��1�֣�����2��2CuO + C ����2Cu + CO2��(2��)����ɫ��������ʧ���д������ݲ�������Һ����ɫ����ɫ(2��)����������㼴�����֣���3��25.6��2�֣�.
��������
�����������1���ɼ�ʽ̼��ͭ[Cu2(OH)2CO3]��֪�����Ԫ��Ϊͭ�������⡢̼����Ԫ�أ���2����ʽ̼��ͭ���ȷֽ����ɵ�������������Ϊ��ɫ�����������ͭ��ľ̿���л�ԭ�ԣ����ڸ���������������ͭ��Ӧ���ɶ�����̼�����ͭ���������ѧ����ʽ��Ԥ��ʵ����������ˮ����ɫ��ĩ��ʽ̼��ͭ����ʧ���õ���ɫ��Һ���������ݲ�������4�����������غ㶨�ɿ�֪44.4g Cu2(OH)2CO3�к��е�ͭԪ�ص�������44.4g��![]() =25.6g����Ϊ�õ���ͭ������.
=25.6g����Ϊ�õ���ͭ������.

 һ��һ��һ��ͨϵ�д�
һ��һ��һ��ͨϵ�д� �㽭֮��ѧҵˮƽ����ϵ�д�
�㽭֮��ѧҵˮƽ����ϵ�д� ��Ч���ܿ�ʱ��ҵϵ�д�
��Ч���ܿ�ʱ��ҵϵ�д�