题目内容
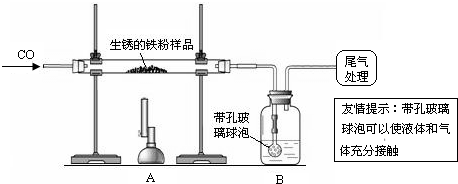
还原性铁粉在潮湿的空气中容易生锈.现有10克生锈的铁粉样品,某兴趣小组同学按如图所示装置进行实验,测定该样品中氧化铁的质量分数(铁锈按氧化铁处理,).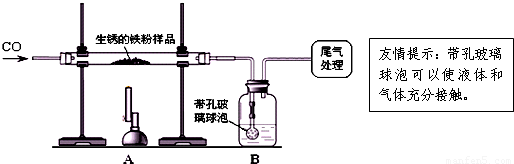
(1)装置A中反应的化学方程式是 .
(2)某同学欲通过B装置反应前后的质量变化,测定该样品中氧化铁的质量分数.B中的最佳试剂是 (填序号),实验时B中反应的化学方程式是 .
①澄清石灰水 ②氢氧化钠浓溶液 ③稀盐酸 ④水
(3)上述实验过程中,CO气体除作为反应物外,还能起到的作用是:
①实验开始时,排尽装置中的空气,防止加热时发生爆炸;
②停止加热后,防止A中生成物被氧化;
③将A装置中的CO2送入B装置的溶液中;
④ .
(4)完全反应后,甲同学称得铁粉的质量为8.8克,同时测得装置B增重3.3克,则生锈的铁粉样品中含氧化铁的质量分数为 .(不考虑空气中二氧化碳的影响)
【答案】分析:(1)运用一氧化碳高温条件下和氧化铁反应生成铁和二氧化碳解答.
(2)运用氢氧化钠易溶于水且能和二氧化碳反应生成碳酸钠和水,氢氧化钙微溶于水解答.
(3)运用一氧化碳还原氧化铁的性质解答.
(4)根据3CO+Fe2O3 2Fe+3CO2计算即可解答.
2Fe+3CO2计算即可解答.
解答:解:(1)一氧化碳高温条件下和氧化铁反应生成铁和二氧化碳,故答案:3CO+Fe2O3 2Fe+3CO2.
2Fe+3CO2.
(2)氢氧化钠易溶于水且能和二氧化碳反应生成碳酸钠和水,而氢氧化钙微溶于水,二氧化碳能使澄清的石灰水变浑浊,所以吸收二氧化碳一般选用氢氧化钠检验二氧化碳选用澄清石灰水.题中B是为了吸收二氧化碳,故答案:②CO2+2NaOH=Na2CO3+H2O
(3)一氧化碳还原氧化铁生成铁和二氧化碳,故答案:和生锈的铁粉中铁锈的主要成分氧化铁反应.
(4)设10g铁粉中氧化铁的质量为x
3CO+Fe2O3 2Fe+3CO2
2Fe+3CO2
160 132
x 3.3g
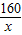 =
=
x=4g
铁粉中氧化铁的质量分数为: ×100%=40%
×100%=40%
故答案:8铁粉中氧化铁的质量分数为40%.
点评:本题对铁粉中氧化铁的含量进行探究考查,只要明白运用氧化铁和一氧化碳反应的生成物二氧化碳的质量即为装置B反应前后增加的质量解答就会找到突破口.
(2)运用氢氧化钠易溶于水且能和二氧化碳反应生成碳酸钠和水,氢氧化钙微溶于水解答.
(3)运用一氧化碳还原氧化铁的性质解答.
(4)根据3CO+Fe2O3
 2Fe+3CO2计算即可解答.
2Fe+3CO2计算即可解答.解答:解:(1)一氧化碳高温条件下和氧化铁反应生成铁和二氧化碳,故答案:3CO+Fe2O3
 2Fe+3CO2.
2Fe+3CO2.(2)氢氧化钠易溶于水且能和二氧化碳反应生成碳酸钠和水,而氢氧化钙微溶于水,二氧化碳能使澄清的石灰水变浑浊,所以吸收二氧化碳一般选用氢氧化钠检验二氧化碳选用澄清石灰水.题中B是为了吸收二氧化碳,故答案:②CO2+2NaOH=Na2CO3+H2O
(3)一氧化碳还原氧化铁生成铁和二氧化碳,故答案:和生锈的铁粉中铁锈的主要成分氧化铁反应.
(4)设10g铁粉中氧化铁的质量为x
3CO+Fe2O3
 2Fe+3CO2
2Fe+3CO2160 132
x 3.3g
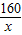 =
=
x=4g
铁粉中氧化铁的质量分数为:
 ×100%=40%
×100%=40%故答案:8铁粉中氧化铁的质量分数为40%.
点评:本题对铁粉中氧化铁的含量进行探究考查,只要明白运用氧化铁和一氧化碳反应的生成物二氧化碳的质量即为装置B反应前后增加的质量解答就会找到突破口.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
还原性铁粉在潮湿的空气中容易生锈.现有m1g生锈的铁粉样品,某兴趣小组同学按下图所示装置进行实验,测定该样品中氧化铁的质量分数(铁锈按氧化铁处理).
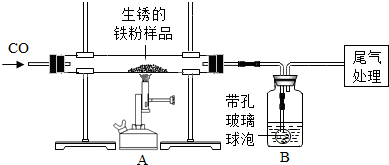

| 友情提示:带孔玻璃球泡可以使液体和气体充分接触(1)装置A中反应的化学方程式是 (2)某同学欲通过B装置反应前后的质量变化,测定该样品中氧化铁的质量分数. B中的最佳试剂是 ①澄清石灰水 ②氢氧化钠浓溶液 ③稀盐酸 ④水 (3)上述实验过程中,CO气体除作为反应物外,还能起到的作用是:①实验开始时,排尽装置中的空气,防止加热时发生爆炸;②停止加热后,防止A中生成物被氧化,B中的溶液倒吸入A中;③ (4)完全反应后,甲同学称得铁粉的质量为m2g,同时测得装置B增重m3g,则铁粉样品中氧化铁的质量分数为
还原性铁粉在潮湿的空气中容易生锈.现有m1g生锈的铁粉样品,某兴趣小组同学按下图所示装置进行实验,测定该样品中氧化铁的质量分数(铁锈按氧化铁处理).

|