题目内容
现有20g溶质质量分数为10%的氯化钠溶液,要使其溶质的质量分数达到20%,可采用的方法是( )A.蒸发12g水
B.蒸发10g水
C.加入2.5g氯化钠
D.加入1.8g氯化钠
【答案】分析:根据增大溶质的质量分数的两种常见的途径可知,蒸发溶剂或增加溶质都可使溶质的质量分数变大来进行计算.
解答:解:若蒸发溶剂使溶质的质量分数变大,设蒸发水的质量为xg,
根据蒸发前后溶质的质量不变,得
20g×10%=(20g-x)×20%
解得x=10g,
即蒸发10g水可使溶质的质量分数达到20%,则B正确;
若增加溶质,设增加的溶质的质量为yg,
根据混合前的溶质质量等于混合后溶液中的溶质质量,得
20g×10%+y=(20g+y)×20%,
解得y=2.5g,
即增加2.5g溶质可使溶质的质量分数达到20%,则C正确;
故选BC.
点评:本题考查增大溶质质量分数的方法和相关计算,学生应熟悉溶质质量分数变大的常见方法并能进行简单计算.
解答:解:若蒸发溶剂使溶质的质量分数变大,设蒸发水的质量为xg,
根据蒸发前后溶质的质量不变,得
20g×10%=(20g-x)×20%
解得x=10g,
即蒸发10g水可使溶质的质量分数达到20%,则B正确;
若增加溶质,设增加的溶质的质量为yg,
根据混合前的溶质质量等于混合后溶液中的溶质质量,得
20g×10%+y=(20g+y)×20%,
解得y=2.5g,
即增加2.5g溶质可使溶质的质量分数达到20%,则C正确;
故选BC.
点评:本题考查增大溶质质量分数的方法和相关计算,学生应熟悉溶质质量分数变大的常见方法并能进行简单计算.

练习册系列答案
相关题目
为了测定某石灰石的纯度(其中杂质不溶与水,不与盐酸反应,高温时不发生分解反应)现取用2g这种石灰石样品,用实验室现有的未知溶质质量分数的稀盐酸20g分4次加入,充分反应后,经过滤、干燥等操作后称量,每次稀盐酸用量及剩余固体质量见下表:
(1)表中m为 g
(2)该石灰石样品的纯度为 .
(3)哪一次盐酸有剩余 .
(4)所用稀盐酸溶质质量分数为 .
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入5g | 1.5g |
| 第二次加入5g | 1.0g |
| 第三次加入5g | m |
| 第四次加入5g | 0.3g |
(2)该石灰石样品的纯度为
(3)哪一次盐酸有剩余
(4)所用稀盐酸溶质质量分数为
现有氧化铜和铜的混合物,对其成分进行分析.取20g此样品,向其中分五次加入相同 溶质质量分数的稀硫酸,使之充分反应.每次所用稀硫酸的质量及剩余固体的质量记录于下表:(反应的化学方程式:CuO+H2SO4=CuSO4+H2O)
试回答下列问题:
(1)上述表格中m的值为 ;
(2)20g样品中CuO的质量分数为 ;
(3)计算所加入稀硫酸中硫酸的质量分数是多少?
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入稀硫酸的质量/g | 40 | 40 | 40 | 40 | 40 |
| 充分反应后剩余固体质量/g | 16 | 12 | 8 | 6 | m |
(1)上述表格中m的值为
(2)20g样品中CuO的质量分数为
(3)计算所加入稀硫酸中硫酸的质量分数是多少?
已知石灰石中的杂质既不溶于水,又不与酸反应,高温时也不分解.为了测定石灰石中碳酸钙的质量分数,化学兴趣小组的同学取用了2g石灰石样品,用实验室现有的未知溶质质量分数的稀盐酸20g分四次加入,充分反应后,过滤、干燥再称量,每次使用稀盐酸的质量及剩余固体的质量见下表:
计算:(1)该石灰石样品中碳酸钙的质量分数.
(2)所用稀盐酸中溶质质量分数.
| 稀盐酸用量 | 剩余固体质量 |
| 第一次加入5g | 1.5g |
| 第二次加入5g | 1.0g |
| 第三次加入5g | 0.5g |
| 第四次加入5g | 0.3g |
(2)所用稀盐酸中溶质质量分数.
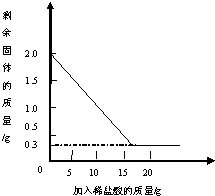 化学兴趣小组同学在综合实践活动中了解到,某石灰厂有一批石灰石原料,其中含有的杂质是二氧化硅(二氧化硅不溶于水,不能与盐酸反应,高温时不发生分解反应).为了测定该石灰石的纯度,兴趣小组同学取用2g这种石灰石样品,用实验室现有的未知溶质质量分数的稀盐酸20g分4次加入,充分反应后,经过滤、干燥等操作后称量,每次稀盐酸用量及剩余固体的质量见下表,利用实验数据绘制的图象见下图.(保留一位有效数字)
化学兴趣小组同学在综合实践活动中了解到,某石灰厂有一批石灰石原料,其中含有的杂质是二氧化硅(二氧化硅不溶于水,不能与盐酸反应,高温时不发生分解反应).为了测定该石灰石的纯度,兴趣小组同学取用2g这种石灰石样品,用实验室现有的未知溶质质量分数的稀盐酸20g分4次加入,充分反应后,经过滤、干燥等操作后称量,每次稀盐酸用量及剩余固体的质量见下表,利用实验数据绘制的图象见下图.(保留一位有效数字)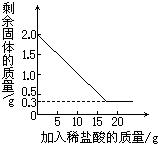 某化学兴趣小组在综合实践活动中了解到,石灰厂有一批石灰石原料,其中含有的杂质是二氧化硅(二氧化硅不溶于水,不能与盐酸反应,高温时不发生分解反应).为了测定该石灰石的纯度,兴趣小组取2g这种石灰石样品于小烧杯中,用实验室现有的未知溶质质量分数的稀盐酸20g分4次加入,充分反应后经过滤、干燥后称量,每次稀盐酸用量及剩余固体的质量见下表,利用实验数据绘制的图象如图.
某化学兴趣小组在综合实践活动中了解到,石灰厂有一批石灰石原料,其中含有的杂质是二氧化硅(二氧化硅不溶于水,不能与盐酸反应,高温时不发生分解反应).为了测定该石灰石的纯度,兴趣小组取2g这种石灰石样品于小烧杯中,用实验室现有的未知溶质质量分数的稀盐酸20g分4次加入,充分反应后经过滤、干燥后称量,每次稀盐酸用量及剩余固体的质量见下表,利用实验数据绘制的图象如图.