题目内容
实验室有失去标签的下列化肥:碳酸氢铵、硫酸铵、磷矿粉、氯化钾.现要对这四种化肥进行鉴别.
(1)请填写下列实验报告:
| 实验操作 | 实验现象 | 实验结论 |
| ①观察药品的颜色 | 有一瓶呈灰色 | 该化肥是 |
| ②打开三瓶颜色为白色的化肥的瓶盖,闻气味 | 有一瓶有强烈的刺激性气味 | 该化肥是 |
| ③取少许剩余的两种化肥,分别加入少量熟石灰,混合研磨,闻气味 | 有刺激性气味 | 该化肥是 (填化学式) |
| 无刺激性气味 | |
(3)反思:由实验②可知,该化肥要保存在 处;由实验③可以发现,在农业生产中, (“钾肥”、“磷肥”、“铵态氮肥”)不能与碱性肥料一起施用。
(1)磷矿粉;碳酸氢铵或NH4HCO3;(NH4)2SO4;
(2)取样品分别于试管中加水溶解,滴入硝酸钡溶液(或氯化钡)溶液,有白色沉淀产生的是硫酸铵,无明显现象的是氯化钾; (3)阴凉;铵态氮肥
解析试题分析:(1)磷矿粉为灰色固体,碳酸氢铵有刺激性气味,而铵态氮肥可以和熟石灰反应生成氨气,可以举出解答该题;①磷矿粉为灰色固体,所以呈灰色的为磷矿粉;②碳酸氢铵易分解,分解的产物有刺激性气味,所以有刺激性气味为碳酸氢铵;③铵态氮肥可以和熟石灰反应生成氨气,所以有刺激性气味产生的为硫酸铵,其化学式为:(NH4)2SO4;
(2)根据氯化钾和硫酸铵的性质来进行解答。硫酸铵可以和氯化钡溶液反应生成白色的沉淀,所以可以用氯化钡溶液来区分硫酸铵和氯化钾,具体操作为:取样品分别于试管中加水溶解,滴入氯化钡溶液,有白色沉淀产生的是硫酸铵,无明显现象的是氯化钾;
(3)根据实验可以知道该化肥容易分解,所以应该保存在阴凉干燥处,而铵态氮肥容易和碱性物质反应,所以不能和碱性肥料一起使用,可以据此解答。根据实验可以知道该化肥容易分解,所以应该保存在阴凉干燥处,而铵态氮肥容易和碱性物质反应,所以不能和碱性肥料一起使用。
考点:考查化肥的简易鉴别;铵态氮肥的检验

 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案在老师的指导下,同学们进行了有趣的化学实验探究:
一、测定空气中氧气含量
图1所示的是小亮同学用红磷在空气中燃烧的测定方法.过程是:
第1步:将集气瓶容积划分为五等份,并做好标记.
第2步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧。
第3步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的1/5.请回答下列问题:

①第2步红磷燃烧时的现象 ,
化学反应表达式: 。
②实验完毕,若进入集气瓶中水的体积不到总容积的1/5,
你认为导致这一结果的原因可能是 。
A、集气瓶底部的水占了一部分体积
B、红磷过少
C、红磷没有燃烧完就急着打开了止水夹
③小博同学对实验进行反思后,提出了改进方法(如图2所示),小博在正式开始实验前,夹紧弹簧夹,将注射器活塞从20mL刻度处推至15mL处,然后松开活塞,观察到活塞返回至20mL刻度处.该操作的主要目的是 ,你认为改进后的优点是 。
二、小余阅读课外资料得知:双氧水分解除了用二氧化锰(MnO2)还可用氧化铜(CuO)等物质作催化剂,于是他对氧化铜产生了探究兴趣。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小余以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验
的因素均忽略)
| 实验序号 | 氯酸钾质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g | |
①上述实验应测量的“待测数据”是 。
②若实验②比实验①的“待测数据”更 (填“大”或“小”),说明氧化铜能加快氯酸钾的分解。
③将实验②反应剩余的固体取出后经洗涤、干燥,再次精确称量得到0.5g黑色粉末,这样做的目的是 ,小余同学认为氧化铜肯定是氯酸钾分解的催化剂,但小淳同学对此提出了异议,小淳同学设计了如下实验:
将第二次精确称量得到的0.5g黑色粉末和1.2g氯酸钾混合放入试管中,加热,伸入带火星木条,发现木条很快复燃。
小淳同学这样做目的是 ,
【预期结论】氧化铜也能作氯酸钾的催化剂。
【评价设计】你认为小余设计实验③和实验②对比的目的是 ;写出实验②反应的表达式 。
三、有趣的改进实验
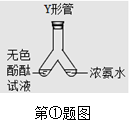
①小晴同学学了分子性质这节内容后,改进了书本上探究分子运动的实验。小晴同学找来废弃的医疗用品-----微型Y 形管,设计如图1所示实验,她进行该实验是为了探究 ,实验过程中能看到的现象是 ,小晴同学设计的实验优点是 。
②利用如图装置进行“硫燃烧”的实验:用气卿(能不断鼓入空气的装置)不断地向弯型具支试管中鼓入空气,同时用酒精灯给硫粉加热至燃烧,移去酒精灯,可观察到微弱的淡蓝色火焰;然后停止鼓入空气,再用酒精灯给高锰酸钾加热,使硫在纯氧中继续燃烧,观察到 火焰。
写出实验中硫磺燃烧的化学反应表达式: ,该实验装置的主要优点是在消除有害气体对环境污染的前提下有利于 .你推断烧杯中的氢氧化钠溶液的 作用是 。

为进一步研究高锰酸钾的分解产物,某兴趣小组同学查阅资料,并取一定质量的高锰酸钾加热使之完全分解,然后分别进行了以下三个实验。
【实验内容】:
| 编号 | 实验内容 | 实验现象 | 实验结论 |
| 1 | 取反应后固体剩余物0.2g加入5mL 6%的H2O2溶液中 | 剧烈反应,放出大量热量,产生大量气体 | 固体剩余物中的MnO2对H2O2分解有催化作用 |
| 2 | 取0.2gMnO2加入5mL a (H2O2溶液的质量分数)的H2O2溶液中 | 平稳反应,放出热量,持续产生气体 | MnO2对H2O2分解有催化作用 |
| 3 | 取反应后固体剩余物1.0g加入足量水中,充分溶解,过滤 | 固体完全溶解,滤纸上无黑色固体残余物 | 固体剩余物中无 b |
【实验分析】
(1)完成上表中的填空内容:a 、b ;
(2)实验2的目的是 ;
(3)同学们经过讨论,认为实验1的结论不正确,理由是 ;
【查阅资料】
Ⅰ、KMnO4受热分解时,在某条件下可能发生以下两个反应:
①6KMnO4
 2K2MnO4+K2Mn4O8+4O2↑
2K2MnO4+K2Mn4O8+4O2↑ ②KMnO4
 KMnO2+O2↑
KMnO2+O2↑Ⅱ、相对分子质量:(KMnO4:158 O2:32)
(4)16gKMnO4中氧元素的质量为 ;加热使之完全分解,若完全发生反应①,生成O2的质量为 ;若同时发生反应①②,生成O2的质量范围是 。(保留二位小数。提示:依据质量守恒定律观察)
某研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
[假设] H2O2生成O2的快慢与催化剂种类有关
[实验方案]常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量MnO2和红砖粉,测量各生成一瓶(相同体积)O2所需的时间。
[试验记录]
| 试验编号 | 1 | 2 |
| 反应物 | 6% H2O2 | 6% H2O2 |
| 催化剂 | 1g红砖 | 1gMnO2 |
| 时间(秒) | 152 S | 35 S |
[结论]
该探究过程得出的结论是 ,
[反思]一个成员说“该实验还不能证明红砖粉可以做该反应的催化剂,若要证明红砖粉是该反应的催化剂,还需要增加试验来验证”,你认为还要增加的实验是证明它们在化学反应前后的 和_____ 是否改变。
[拓展]H2O2生成O2的快慢还与哪些因素有关?
[假设]
(10分)钛(Ti)是一种重要的航天金属材料.某学习小组对三种金属Ti、Al、Cu的金属活动性顺序进行探究.过程如下:
提出假设:a.Ti金属活动性比Al强 b.Al金属活动性比Cu强
查阅资料:钛能与盐酸反应.
实验设计:同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量的稀盐酸中反应,观察现象.
操作分析:三种金属加入盐酸前都先用砂布将表面擦光亮,其目的是
A.除去氧化膜,利于直接反应
B.使表面光亮,易观察现象
C.使反应金属温度相同,易反应
| 金属 | Ti | Al | Cu |
| 与盐酸反应现象 | 反应缓慢 | 反应剧烈 | 无明显现象 |
实验现象,实验结论:
(1)原假设中 不正确(填“a”、“b”或“a、b”).
(2)三种金属的金属活动性由强至弱的顺序为 。
结论应用:能否用铝制容器来盛装波尔多液(含硫酸铜), (填“能”或“否”),理由是 。



