题目内容
(2010?乌鲁木齐)下列氮肥中,氮元素的质量分数最大的是( )
【答案】分析:化合物中某元素的质量分数= ×100%
×100%
尿素中氮的质量分数为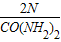 ,硫酸铵中氮的质量分数为:
,硫酸铵中氮的质量分数为: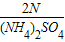 ,硝酸铵中氮的质量分数为
,硝酸铵中氮的质量分数为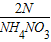 ,硝酸钾中氮的质量分数为
,硝酸钾中氮的质量分数为 ,观察可知,把硝酸钾中氮的质量分数的计算式分子分母同乘以2,则分子与前三者相同,所以,只要算出分母,即可比较大小.
,观察可知,把硝酸钾中氮的质量分数的计算式分子分母同乘以2,则分子与前三者相同,所以,只要算出分母,即可比较大小.
解答:解:尿素中氮的质量分数为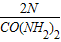 ,硫酸铵中氮的质量分数为:
,硫酸铵中氮的质量分数为: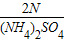 ,硝酸铵中氮的质量分数为
,硝酸铵中氮的质量分数为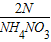 ,硝酸钾中氮的质量分数为
,硝酸钾中氮的质量分数为 =
=
在分子相同的情况下,分母越小,结果越大.
计算可知,尿素的相对分子质量为60,硫酸铵的相对分子质量为132,硝酸铵的相对分子质量80,硝酸钾的相对分子质量乘以2为202.可见,尿素中氮元素的质量分数最大.
故选A
点评:此题要求比较元素质量分数的高低.运用公式逐一计算也能通过计算结果比较,但太繁琐.快速解题的方法是变式求同法.把公式变成为易于分析的形式,一般不看转化后的相同部分,而去分析比较差异的部分,即可得出结论.
 ×100%
×100%尿素中氮的质量分数为
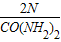 ,硫酸铵中氮的质量分数为:
,硫酸铵中氮的质量分数为: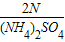 ,硝酸铵中氮的质量分数为
,硝酸铵中氮的质量分数为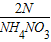 ,硝酸钾中氮的质量分数为
,硝酸钾中氮的质量分数为 ,观察可知,把硝酸钾中氮的质量分数的计算式分子分母同乘以2,则分子与前三者相同,所以,只要算出分母,即可比较大小.
,观察可知,把硝酸钾中氮的质量分数的计算式分子分母同乘以2,则分子与前三者相同,所以,只要算出分母,即可比较大小.解答:解:尿素中氮的质量分数为
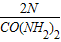 ,硫酸铵中氮的质量分数为:
,硫酸铵中氮的质量分数为: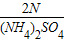 ,硝酸铵中氮的质量分数为
,硝酸铵中氮的质量分数为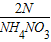 ,硝酸钾中氮的质量分数为
,硝酸钾中氮的质量分数为 =
=
在分子相同的情况下,分母越小,结果越大.
计算可知,尿素的相对分子质量为60,硫酸铵的相对分子质量为132,硝酸铵的相对分子质量80,硝酸钾的相对分子质量乘以2为202.可见,尿素中氮元素的质量分数最大.
故选A
点评:此题要求比较元素质量分数的高低.运用公式逐一计算也能通过计算结果比较,但太繁琐.快速解题的方法是变式求同法.把公式变成为易于分析的形式,一般不看转化后的相同部分,而去分析比较差异的部分,即可得出结论.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目