题目内容
小明同学在实验室用大理石和稀盐酸反应制取二氧化碳完毕后,对废液中溶质的成分产生了兴趣.请你一同参与探究并回答下列问题:
【提出问题】废液中的溶质是什么物质?
【作出猜想】小明同学认为废液中溶质只有氯化钙.你认为还可能有的溶质是 (填化学式).
【查阅资料】氯化钙溶液呈中性.
【实验与结论】
(1)小明同学取少量废液于试管中,滴入几滴无色酚酞试液后,酚酞不变色,于是小明同学认为自己的猜想是正确的.
(2)你认为小明同学的实验 (填“能”或“不能”)证明他的猜想,理由是 .
(3)如果要证明你的猜想是正确的,你选择的试剂是 ,实验中可以看到的现象是 .
【拓展与应用】
(1)实验证明你的猜想是正确的,要想处理废液只得到氯化钙溶液,你的实验步骤是 .
(2)通过以上探究,如果该废液未经处理直接倒入下水道,可能造成的危害是 (写一条).
【交流与反思】在分析化学反应后所得物质的成分时,除了考虑生成物外,还需要考虑 .
【作出猜想】HCl
【实验与结论】
(2)不能;盐酸显酸性,不能使酚酞试液变色
(3)石蕊试液;石蕊试液变红色
【拓展与应用】
(1)向废液中加入碳酸钙,当不再产生气泡时,停止加入碳酸钙,过滤既得只含有氯化钙的废液
(2)腐蚀下水道
【交流与反思】反应物是否过量
解析试题分析:【作出猜想】
小明同学认为废液中溶质只有氯化钙.你认为还可能有的溶质是氯化氢,化学式是HCl.
故填:HCl.
【实验与结论】
(2)你认为小明同学的实验不能证明他的猜想,理由是盐酸显酸性,不能使酚酞试液变色.
故填:不能;盐酸显酸性,不能使酚酞试液变色.
(3)如果要证明你的猜想是正确的,你选择的试剂是石蕊试液,实验中可以看到的现象是石蕊试液变红色.
故填:石蕊试液;石蕊试液变红色.
【拓展与应用】
(1)实验步骤是:向废液中加入碳酸钙,当不再产生气泡时,停止加入碳酸钙,过滤既得只含有氯化钙的废液.
故填:向废液中加入碳酸钙,当不再产生气泡时,停止加入碳酸钙,过滤既得只含有氯化钙的废液.
(2)通过以上探究,如果该废液未经处理直接倒入下水道,可能造成的危害是腐蚀下水道.
故填:腐蚀下水道.
【交流与反思】
在分析化学反应后所得物质的成分时,除了考虑生成物外,还需要考虑反应物是否过量.
故填:反应物是否过量.
考点:实验探究物质的组成成分以及含量;混合物的分离方法;酸碱指示剂及其性质;酸的化学性质.
点评:化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力.

不少同学都被蚊虫叮咬过,感觉又痛又痒.同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤.课外兴趣小组同学决定对蚁酸进行探究。
【提出问题】蚁酸的成分是什么?它有什么性质?
【查阅资料】蚁酸是一种有机酸,化学名称叫做甲酸,化学式为HCOOH;蚁酸在一定条件下会分解生成两种氧化物。
【实验探究一】探究蚁酸的酸性。
(1)向盛有蚁酸溶液的试管中滴加紫色石蕊试液,观察到溶液颜色变成 色,说明蚁酸溶液显酸性;
(2)将锌粒放入盛有蚁酸溶液的试管中,有气泡产生,该气体是 。
【实验探究二】探究蚁酸分解的两种产物。
(1)小芳同学根据蚁酸中含有 元素,推测出生成物中含有水;
(2)另一种生成物是气体,小敏提出两种猜想:
猜想①:该气体是CO2 猜想②:该气体是 他们将蚁酸分解产生的气体通过如下装置(铁架台已略去),观察现象。
Ⅰ.实验时装置A中无明显变化,则猜想① (填“成立”或“不成立”);
Ⅱ.装置B中的现象是 ,装置C中发生反应的化学方程式为 。
【讨论交流】从环保角度看,该装置的缺陷是 ,处理的方法是 。
【拓展延伸】
(1)当你被蚊虫叮咬后,在叮咬处涂抹一些物质可减轻痛痒.下列物质中,你不会选择的物质是 。
| A.氨水 | B.食醋 | C.肥皂水 | D.苏打水 |
小丽在探究碱的化学性质时,将稀盐酸滴入到氢氧化钠溶液中,意外地看到有气泡产生,她认为氢氧化钠溶液已经变质了.用化学方程式表示氢氧化钠溶液变质的原因: .
【提出问题】变质后的氢氧化钠溶液中的溶质是什么?
【猜想假设】小丽对变质后的氢氧化钠溶液中的溶质成分做出了两种猜想:
猜想一: ;猜想二: .
【实验设计】为验证上述猜想哪个正确,小丽设计了如下方案:取少量氢氧化钠溶液样品于试管中,滴加几滴无色酚酞溶液,观察溶液颜色变化.小红认为小丽的实验方案不合理,理由是: .
【实验与结论】小红另外设计并完成了实验,请你帮她填写下面的实验报告:
| 实验步骤 | 实验现象 | 结论 |
| 步骤1:取少量氢氧化钠溶液样品于试管中,向其中滴加过量的 | | 猜想一 正确 |
| 步骤2: | |
某化学兴趣小组的同学往氢氧化钠溶液中滴加稀盐酸时,没有看到明显现象.
【提出问题】氢氧化钠与盐酸是否发生了化学反应?
【查阅资料】酸与碱发生中和反应会放出热量.
【实验设计】甲、乙、丙三位同学分别设计了如下实验方案,请你帮他们完成实验报告.
| 同学 | 实验操作 | 现象 | 结论 |
| 甲 |  | 溶液由红色变成 | 氢氧化钠与盐酸发生了化学反应,反应的化学方程式为 |
| 乙 | 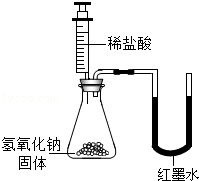 | U型玻璃管中 边的红墨水液面下降(所加稀盐酸的体积忽略不计) | 氢氧化钠与盐酸发生了化学反应 |
| 丙 | 用 测定氢氧化钠溶液的pH,向其中滴加足量稀盐酸,再测定溶液的pH | 最后溶液的pH (填“≥7”、“≤7”、“不变” | 氢氧化钠与盐酸发生了化学反应 |
【评价反思】你认为实验设计方案不合理的同学是 ,理由是 .
【拓展延伸】另有一位同学向自己配制的氢氧化钠溶液中滴加酚酞试液时,溶液变红色,可是红色即可消失了,出现此意外情况的原因是 (填以下序号).
A.所用的酚酞试液是变质的
B.所用的氢氧化钠溶液浓度太小
C.氢氧化钠溶液吸收了空气中二氧化碳
小东、小林和小雨同学对氢氧化钠溶液使酚酞溶液变红的现象很感兴趣,决定做实验进行探究:氢氧化钠溶液中到底是哪一种粒子使酚酞溶液变红?实验中可供使用的用品有盐酸、氯化钠溶液、氯化钙溶液、氢氧化钠溶液、碳酸钠溶液、酚酞溶液及若干支试管。
【提出假设】假设(1):使酚酞溶液变红的是H2O。
假设(2):使酚酞溶液变红的是Na+。
假设(3):使酚酞溶液变红的是________。
小东认为不做实验即可说明假设(1)不成立,原因是 ___________________。
【实验验证】(完成下列实验操作、实验现象及实验结论)
| 实验步骤 | 实验操作 | 实验现象 | 实验结论 |
| (1) | 向装有氢氧化钠溶液的试管中滴加酚酞溶液 | 溶液变为红色 | |
| (2) | | | |
小雨认为向实验步骤(1)后的试管中加入盐酸也可得出正确结论,你同意她的观点吗?_________(填“同意”或“不同意”)。
【实验拓展】
小林将酚酞溶液滴入碳酸钠溶液中,发现溶液也变红。他们经过分析、讨论、归纳,得出的结论是_______。
对物质进行归类整理是化学学习的一种重要方法,下列归类关系不相符的是( )
| A.空气、海水﹣﹣纯净物 | B.白磷、红磷﹣﹣可燃物 |
| C.不锈钢、铜﹣﹣金属材料 | D.合成橡胶、塑料﹣﹣有机合成材料 |
 C+2MgO ②3Mg+N2
C+2MgO ②3Mg+N2 Mg3N2
Mg3N2
