题目内容
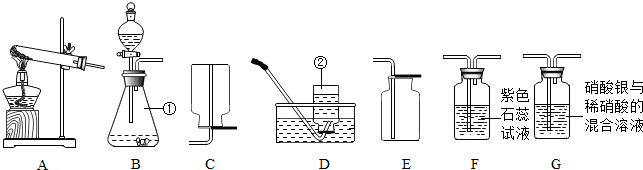
17、某班同学在实验室选用下图装置进行CO2的制取和验证性质的分组实验.

(1)实验室制取和收集CO2应该选择
(2)若将制得的CO2通入澄清的石灰水中,未见浑浊.小张认为可能是错用了较浓的盐酸,使制得的CO2中混入了氯化氢气体.为了验证小张的想法,甲、乙两组同学选择图中的G或H装置与发生装置连接进行实验.你认为:
①甲组同学选择G装置,他们
②乙组同学选择H装置,他们

(1)实验室制取和收集CO2应该选择
C与E
装置(填装置编号),反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑
.(2)若将制得的CO2通入澄清的石灰水中,未见浑浊.小张认为可能是错用了较浓的盐酸,使制得的CO2中混入了氯化氢气体.为了验证小张的想法,甲、乙两组同学选择图中的G或H装置与发生装置连接进行实验.你认为:
①甲组同学选择G装置,他们
不能
(填“能”或“不能”)证实这一想法,理由是HCl与CO2溶于水都能使石蕊试液变红
.②乙组同学选择H装置,他们
能
(填“能”或“不能”)证实这一想法,理由是HCl能够生成白色AgCl沉淀,而CO2不会产生白色沉淀
.分析:(1)发生装置主要由反应物的状态和反应条件决定,收集装置主要由气体的密度和溶水性决定;熟记常用的化学方程式.
(2)①根据酸碱指示剂的变色情况进行分析,二氧化碳和水反应生成的碳酸能使紫色的石蕊溶液变红,氯化氢气体的水溶液盐酸也能使紫色的石蕊溶液变红.
②根据酸、碱、盐、的化学性质进行分析,盐酸和硝酸银反应生成氯化银白色沉淀,二氧化碳和硝酸银不反应.
(2)①根据酸碱指示剂的变色情况进行分析,二氧化碳和水反应生成的碳酸能使紫色的石蕊溶液变红,氯化氢气体的水溶液盐酸也能使紫色的石蕊溶液变红.
②根据酸、碱、盐、的化学性质进行分析,盐酸和硝酸银反应生成氯化银白色沉淀,二氧化碳和硝酸银不反应.
解答:解:(1)反应物的状态是固态和液态,反应条件是常温,应选固-液不加热型的发生装置,二氧化碳的密度比空气大,能溶于水,只能用向上排空气法收集;碳酸钙与盐酸反应生成氯化钙、水和二氧化碳.故答案为:C与E;CaCO3+2HCl═CaCl2+H2O+CO2↑
(2)①氯化氢气体的水溶液是盐酸,能使紫色的石蕊溶液变红,二氧化碳和水反应生成碳酸,碳酸也能使紫色的石蕊溶液变红,所以不管二氧化碳中有没有氯化氢气体,紫色的石蕊溶液都会变红,因而不能使用该装置.故答案为:不能;HCl与CO2溶于水都能使石蕊试液变红
②氯化氢气体的水溶液盐酸和硝酸银反应生成不溶于稀硝酸的白色沉淀,而二氧化碳和硝酸银不反应,没有白色沉淀生成,也有可能会生成少量的碳酸银,会造成溶液浑浊,但碳酸银和硝酸反应,浑浊又会消失.所以若使用的是浓盐酸,会看到有白色沉淀生成,若使用的是稀盐酸,将没有白色沉淀生成.故答案为:能;HCl能够生成白色AgCl沉淀,而CO2不会产生白色沉淀
(2)①氯化氢气体的水溶液是盐酸,能使紫色的石蕊溶液变红,二氧化碳和水反应生成碳酸,碳酸也能使紫色的石蕊溶液变红,所以不管二氧化碳中有没有氯化氢气体,紫色的石蕊溶液都会变红,因而不能使用该装置.故答案为:不能;HCl与CO2溶于水都能使石蕊试液变红
②氯化氢气体的水溶液盐酸和硝酸银反应生成不溶于稀硝酸的白色沉淀,而二氧化碳和硝酸银不反应,没有白色沉淀生成,也有可能会生成少量的碳酸银,会造成溶液浑浊,但碳酸银和硝酸反应,浑浊又会消失.所以若使用的是浓盐酸,会看到有白色沉淀生成,若使用的是稀盐酸,将没有白色沉淀生成.故答案为:能;HCl能够生成白色AgCl沉淀,而CO2不会产生白色沉淀
点评:将二氧化碳通入紫色的石蕊溶液,紫色的石蕊溶液会变红,不是二氧化碳显酸性,使紫色的石蕊变红,而是二氧化碳和水反应生成的碳酸使紫色的石蕊溶液变红.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
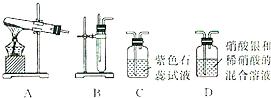 24、某班同学在实验室选用下列装置进行CO2的制取和性质验证的分组实验.
24、某班同学在实验室选用下列装置进行CO2的制取和性质验证的分组实验.