题目内容
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:
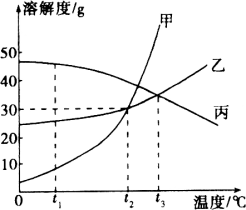
(1)t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是________;
(2)t2℃时,甲和乙的溶解度________(填“相等”或“不相等”);
(3)t2℃时,甲物质的饱和溶液中溶质与溶剂的质量比为________(写最简比);
(4)t3℃时,将乙和丙两种物质的饱和溶液降低到t1℃,所得溶液中溶质的质量分数大小关系为:乙________丙(填“>”“<”或“=”).
【答案】(1)丙 乙 甲 (2)相等 (3)3︰10 (4)<
【解析】(1)由溶解度曲线图可知,t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是丙>乙>甲.
(2)t2℃时,甲和乙的溶解度曲线相交于一点,因此二者溶解度相等.
(3)t2℃时,甲物质的溶解度为30g,甲物质的饱和溶液中溶质与溶剂的质量比为30︰100=3︰10.
(4)将乙和丙两种物质的饱和溶液由t3℃降低到t1℃时,乙的饱和溶液中有晶体析出,溶质质量分数减小;降温时丙的饱和溶液变为不饱和溶液,溶液中的溶质、溶剂质量均不变,溶质质量分数不变,因此所得溶液中溶质的质量分数大小关系为乙<丙.本题解答时应注意以下规律:对溶解度随温度的升高而增大的物质(如本题甲和乙),其饱和溶液降温时一定有晶体析出,溶液中溶质质量分数一定减小;对溶解度随温度的升高而减小的物质(如本题丙),降低温度时其饱和溶液变为不饱和溶液,溶液中溶质的质量分数不变.

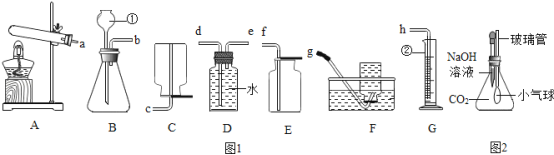
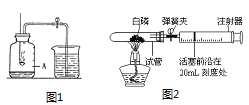
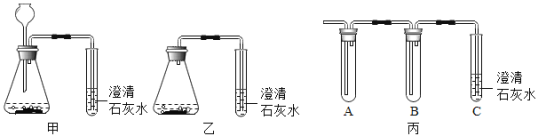
【题目】小敏和小玉在实验室用盐酸和石灰石反应,分别用甲、乙装置(气密性均良好)进行二氧化碳的制取及性质实验,但均未发现澄清石灰水边浑浊.针对此现象,同学们提出了自己的想法.
小敏同学实验时澄清石灰水未变浑浊的原因是_______.
(提出问题)小玉同学实验时澄清石灰水为什么没有变浑浊呢?
(作出猜想)猜想一:澄清石灰水变质.猜想二:反应产生的气体除了有二氧化碳外,还有氯化氢.
(查阅资料)氯化氢气体溶于水形成盐酸.
(实验探究)
实验 | 实验步骤 | 实验现象 | 实验结论 |
实验Ⅰ | 将纯净的CO2通入到该实验所用的澄清石灰水中 | 澄清的石灰水边浑浊 | 猜想一不成立 |
实验Ⅱ | 将反应产生的气体通入到_____ | _____ | 猜想二成立 |
同学们经过讨论发现,用丙装置(如图)在A、B中均加入实验Ⅱ所用试剂即可同时完成上述两个猜想的探究,其中B装置所起的作用是_____.如果看到____现象,则两个猜想都成立.
(实验反思)由实验可知,小玉同学实验时可能错误使用了一种药品,她使用的药品是___.