题目内容
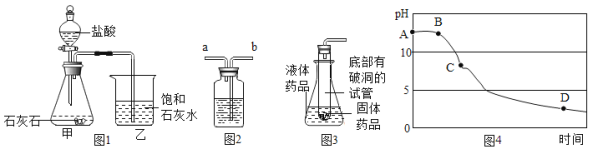
【题目】通过下列实验,不能达到实验目的的是( )

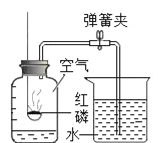
A.图1探究分子在不断运动B.图2粗略测定瓶中氧气的体积
C.图3比较铁、铜、银活动性的强弱D.图4探究CO2的密度和石蕊花变红的原因
【答案】A
【解析】
A、酚酞遇酸不变色,不能探究分子在不断运动,错误;
B、可通过注射器中反应前后水的体积变化,测定瓶中氧气的体积,正确;
C、铜丝在硝酸银溶液中表面会有白色物质生成,说明铜比银活泼,10分钟后放入铁丝,铁丝表面有红色物质生成,说明铁比铜活泼,能比较铁、铜、银活动性的强弱,正确;
D、玻璃管中下面的湿润石蕊花先变色说明二氧化碳密度大于空气密度,而干燥的花不变色,说明变色原因是二氧化碳和水反应生成碳酸导致,能探究CO2的密度和石蕊花变红的原因,正确。故选A。

 阅读快车系列答案
阅读快车系列答案【题目】下列实验设计能达到实验目的的是( )
选项 | 实验目的 | 实验设计 |
A | 除去CO中的少量 | 先通过浓硫酸再通过氢氧化钠溶液 |
B | 除去铁粉中的铜粉 | 加入足量的稀 |
C | 除去 | 加入适量的 |
D | 鉴别 | 加入适量 |
A.AB.BC.CD.D
【题目】小杰同学在复习铁生锈条件时知道,常温下,没有氧气,铁与水几乎不反应。老师告诉同学们,高温下,铁与水蒸气能反应生成一种常见的铁的氧化物和一种气体。小杰很好奇,设计如图所示实验探究铁粉与水蒸气反应后的产物。
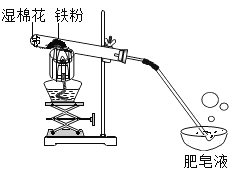
(1)试管尾部放一团湿棉花的目的是___________________。
(2)探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是_________________。
(3)探究试管中剩余固体成分是什么?
(查阅资料)常见的铁的氧化物有FeO(黑色、没有磁性)、![]() 、
、![]() 。
。
(初步验证)试管中固体为黑色,能全部被磁铁吸引。
(猜想与假设)猜想一:剩余固体是![]() ;猜想二剩余固体是__________________。
;猜想二剩余固体是__________________。
(实验探究)
实验操作 | 实验现象结论 |
______________________ | ___________________证明猜想一正确 |
(实验结论)铁和水蒸气反应的化学方程式:___________________。
(反思与交流)该黑色固体不可能是![]() ,理由是___________________。
,理由是___________________。