题目内容
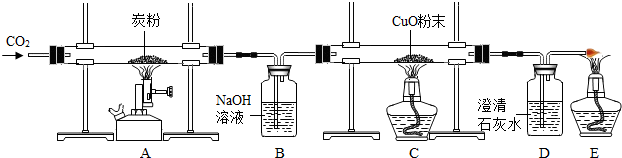
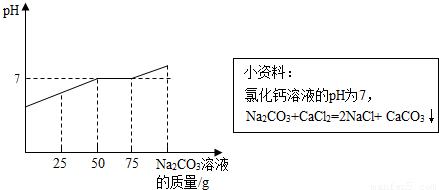
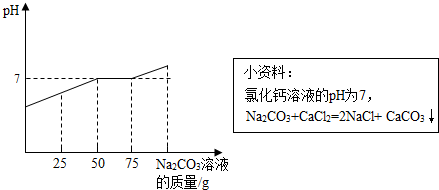
实验制取二氧化碳后,产生大量含有盐酸的废液.为消除酸对水环境的污染,化学兴趣小组做了如下实验:取废液桶上层清液共60g,向其中加入溶质质量分数为21.2%的碳酸钠溶液.所得溶液pH与加入的碳酸钠溶液的质量关系如图所示.
回答下列问题:
(1)处理废液中的盐酸消耗碳酸钠溶液的质量为________.
(2)废液中含氯化钙的质量分数是多少?
解:(1)由图示可知,当碳酸钠溶液质量加到50g时,pH=7,说明此时溶液正好完全中和;
故答案为:50g;
(2)解:设废液中含氯化钙的质量为x,
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 111
(75-50)g×21.2% x
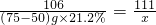
x=5.55g
废液中含氯化钙的质量分数为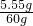 ×100%═9.25%
×100%═9.25%
分析:(1)由图示可知,当碳酸钠溶液质量加到50g时,pH=7,说明此时溶液正好中和;
(2)根据碳酸钠与氯化钙反应的化学方程式,计算出废液中含氯化钙的质量,然后根据“溶质质量分数=溶质质量/溶液质量×100%”即可计算出废液中含氯化钙的质量分数,
点评:本题属于综合计算,主要考查学生运用所学化学知识综合分析和逻辑思维能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
故答案为:50g;
(2)解:设废液中含氯化钙的质量为x,
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 111
(75-50)g×21.2% x
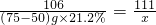
x=5.55g
废液中含氯化钙的质量分数为
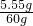 ×100%═9.25%
×100%═9.25%分析:(1)由图示可知,当碳酸钠溶液质量加到50g时,pH=7,说明此时溶液正好中和;
(2)根据碳酸钠与氯化钙反应的化学方程式,计算出废液中含氯化钙的质量,然后根据“溶质质量分数=溶质质量/溶液质量×100%”即可计算出废液中含氯化钙的质量分数,
点评:本题属于综合计算,主要考查学生运用所学化学知识综合分析和逻辑思维能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案
相关题目