题目内容
【题目】芯片是智能家电的核心部件,它是以高纯度的单质(Si)为材料制成的。硅及其氧化物能发生如下反应:
①Si+O2![]() SiO2
SiO2
②Si+2NaOH+X=Na2SiO3+2H2↑
③SiO2+2C![]() Si+2CO↑
Si+2CO↑
④SiO2+Na2CO3![]() Na2SiO3+CO2↑
Na2SiO3+CO2↑
下列说法不正确的是( )
A.反应②中X的化学式为H2O
B.反应③进行中不能有O2存在
C.反应④属于置换反应
D.Si和SiO2在一定条件下可以相互转化
【答案】C
【解析】
A、由质量守恒定律:反应前后,原子种类、数目均不变,进行分析判断;
B、根据碳、一氧化碳均能与氧气反应,进行分析判断;
C、置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应;
D、根据反应①③,进行分析判断。
A、由质量守恒定律:反应前后,原子种类、数目均不变,则每个X分子由2个氢原子和1个氧原子构成,则物质X的化学式为H2O,故选项说法正确;
B、碳、一氧化碳均能与氧气反应,反应③进行中不能有O2存在,故选项说法正确;
C、反应④的生成物均为化合物,不属于置换反应,故选项说法错误;
D、由反应①③可知,Si和SiO2在一定条件下可以相互转化,故选项说法正确。
故选:C。

 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案【题目】小王同学为探究盐酸的化学性质,进行如下探究实验:
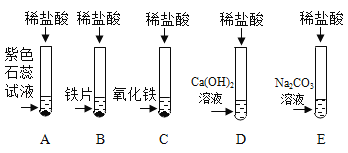
(1)试管C中反应的化学方程式为______________。
(2)小王同学把反应后D、E试管中的溶液倒入一个洁净的烧杯中,观察到先有气泡产生,后有白色沉淀生成。过滤,得到白色沉淀和无色滤液。
从上述实验现象可得,原D试管中反应后溶液的溶质是______________。
小王同学欲探究无色滤液中的溶质成分:
[提出问题]无色滤液的溶质是什么?
[作出猜想]猜想①: NaCl;
猜想②:______________。
猜想③:_____________。
[实验探究]
实验步骤 | 实验现象 | 实验结论 |
①取少量滤液于试管中,滴加少量碳酸钠溶液 | 无明显现象 | 猜想②不成立 |
②另取少量滤液于试管中,滴加少量盐酸 | _____________。 | 猜想③成立 |
[拓展延伸]酸跟盐发生反应的条件是_____________。
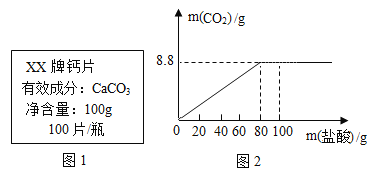
【题目】钙是人体中的常量元素,因缺钙而导致骨质疏松、佝偻病等的患者应在医生的指导下服用钙片。某补钙药剂说明书的部分信息如图1所示。现将100g盐酸分成五等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与关系图如图2.请根据有关信息回答问题。
实验次数 | 第一次 | 第三次 | 第四次 |
加入盐酸的质量(g) | 20 | 20 | 20 |
剩余固体的质量(g) | 35 | a | 20 |
(1)该品牌补钙药剂中CaCO3的质量分数是________,a的数值为________。
(2)该盐酸中溶质的质量分数是多少________?(写出计算过程,计算结果精确至0.1%)