题目内容
【题目】人类的生活离不开水。
①某水厂生产自来水的净化步骤如下:
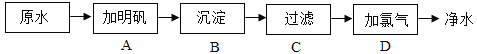
其中为除去难溶性杂质而采取的步骤有_______(填标号),能消毒杀菌的步骤为_______(填标号)。
②图一是电解水杂质,图二是反应示意图 ![]() ”表示氢原子,“
”表示氢原子,“ ![]() ”表示氧原子。
”表示氧原子。
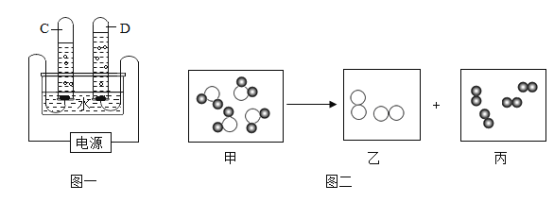
Ⅰ.图二甲乙丙中表示化合物的是_______(填序号),该过程所表示的化学反应属于_______(填一种基本反应类型),发生反应的化学方程式是_______。
Ⅱ.乙所代表的的物质是图一中试管_______(填字母)中产生的气体。
Ⅲ.反应中,乙与丙分子数之比是_______。
Ⅳ.在电解水的过程中,能保持水化学性质的最小微粒是_______(用化学符号表示);检验D管中产物的方法是_______。
【答案】ABC D 甲 分解反应 2H2O![]() 2H2↑+O2↑ D 1:2 H2O 将带火星的木条伸入试管内,木条复燃,则为氧气
2H2↑+O2↑ D 1:2 H2O 将带火星的木条伸入试管内,木条复燃,则为氧气
【解析】
①明矾溶于水形成的胶体能吸附小颗粒不溶性固体杂质,形成大颗粒,沉降过滤能除去不溶性固体大颗粒,故除去难溶性杂质而采取的步骤有ABC,加氯气能消毒杀菌,故能消毒杀菌的步骤为D。
②Ⅰ、电解水生成氢气和氧气,乙丙均是单质,“ ![]() ”表示氧原子,乙是氧气,
”表示氧原子,乙是氧气,![]() ”表示氢原子,丙是氢气,甲是化合物,甲是水,故图二甲乙丙中表示化合物的是甲,该过程所表示的化学反应符合一变多,故属于分解反应,发生反应的化学方程式是2H2O
”表示氢原子,丙是氢气,甲是化合物,甲是水,故图二甲乙丙中表示化合物的是甲,该过程所表示的化学反应符合一变多,故属于分解反应,发生反应的化学方程式是2H2O![]() 2H2↑+O2↑。
2H2↑+O2↑。
Ⅱ. 电解水正极生成氧气,负极生成氢气,“ ![]() ”表示氧原子,乙所代表的的物质是氧气,故乙所代表的的物质是图一中试管D中产生的气体。
”表示氧原子,乙所代表的的物质是氧气,故乙所代表的的物质是图一中试管D中产生的气体。
Ⅲ. 电解水的化学方程式为2H2O![]() O2↑+2H2↑,故反应中,乙与丙分子数之比是1:2。
O2↑+2H2↑,故反应中,乙与丙分子数之比是1:2。
Ⅳ. 在电解水的过程中,水是由水分子构成的,故能保持水化学性质的最小微粒是水分子,化学式为H2O;D管中产物是氧气,故检验D管中产物的方法是将带火星的木条伸入试管内,木条复燃,则为氧气。

【题目】宏宏同学发现上个月做实验用的氢氧化钠溶液忘记了盖瓶塞。对于该溶液是否变质,宏宏邀约几个喜欢探究的同学对此进行了探究。请你一起完成下列实验报告。
(提出问题1)该溶液是否变质?
(实验探究1)
实验步骤 | 实验现象 | 解释与结论 |
取少量该溶液于试管中,滴加足量稀盐酸 | 有______产生 | 说明该溶液已变质,变质的原因是________(用化学方程式表示) |
(提出问题2)该溶液变质程度怎样?
(提出猜想)猜想一:已完全变质,该溶液中溶质只含Na2CO3;
猜想二:部分变质,该溶液中溶质含有__。
(查阅资料)氯化钡溶液呈中性。
(实验探究2)
实验步骤 | 实验现象 | 结论 |
先取少量该溶液于试管中,加入过量氯化钡溶液 | 有______产生 | 猜想______成立 |
静置,取上层清液于另一只试管中,加入2-3滴酚酞溶液 | 上层清液变红 |
(提出问题3)怎样提纯该样品得到纯净的氢氧化钠固体?
(实验探究3)为得到纯净的氢氧化钠固体,同学们取该样品并设计了如图实验方案。
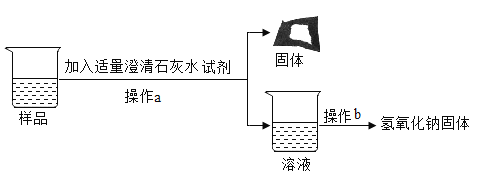
根据实验流程可知,最终所得氢氧化钠固体质量__(填“大于”“小于”或“等于”)变质后样品中氢氧化钠的质量。
(反思交流)在(实验探究2)中加入过量的氯化钡溶液的目的是__。