题目内容
【题目】已知:Al(OH)3沉淀可溶于NaOH溶液,其反应方程式为:Al(OH)3+NaOH═NaAlO2+2H2O,现向100gHCl和AlCl3的混合溶液中逐滴加入质量分数为20%的NaOH溶液,产生沉淀的质量与所加NaOH溶液的质量关系如图所示.回答下列问题: 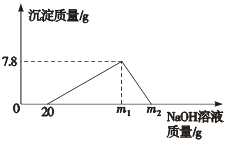
(1)原混合溶液中HCl的质量分数是 .
(2)当沉淀达到最大值时生成NaCl的质量是多少?
(3)m2= .
【答案】
(1)3.65%
(2)解:由于生成的氢氧化铝的质量为7.8g,设生成的氯化钠的质量为z,消耗的氢氧化钠的质量为a
AlCl3+ | 3NaOH= | Al(OH)3↓+ | 3NaCl |
120 | 78 | 175.5 | |
a | 7.8g | z |
![]() =
= ![]() =
= ![]()
a=12g
z=17.55g
当沉淀达到最大值时生成NaCl的质量是5.85g+17.55g=23.4g
(3)100
【解析】解:
由图可以看出和盐酸反应的氢氧化钠溶液的质量为20g,其溶质的质量为20%×20g=4g
设混合溶液中HCl的质量为x,生成的氯化钠的质量为y
HCl+ | NaOH= | NaCl+H2O |
36.5 | 40 | 58.5 |
x | 4g | y |
![]() =
= ![]() =
= ![]()
x=3.65g
y=5.85g
原混合溶液中HCl的质量分数为 ![]() ×100%=3.65%
×100%=3.65%
设和氢氧化铝的氢氧化钠的质量为b
Al(OH)3+ | NaOH═NaAlO2+2H2O |
78 | 40 |
7.8g | b |
![]() =
= ![]()
b=4g
到沉淀完全溶解消耗的氢氧化钠的质量为4g+12g+4g=20g
对应的氢氧化钠溶液的质量为 ![]() =100g.
=100g.
答:(1)原混合溶液中HCl的质量分数是3.65%.(2)当沉淀达到最大值时生成NaCl的质量是23.4g.(3)m2=100.
【考点精析】利用根据化学反应方程式的计算对题目进行判断即可得到答案,需要熟知各物质间质量比=系数×相对分子质量之比.

 全能练考卷系列答案
全能练考卷系列答案【题目】下列实验方案不合理的是( )
选项 | 实验目的 | 所用试剂和方法 |
A | 鉴别浓盐酸和浓硫酸 | 打开瓶塞,观察是否有白雾产生 |
B | 鉴别氯化钡溶液和硝酸钾溶液 | 分别加入硫酸钠溶液 |
C | 除去二氧化碳气体中少量的一氧化碳 | 将气体点燃 |
D | 除去氧化铝粉末中的铝粉 | 在干燥空气中加热 |
A. AB. BC. CD. D