题目内容
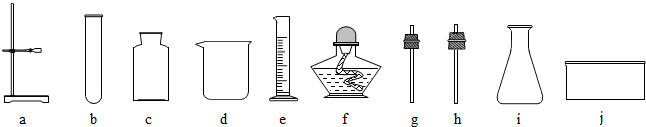
我们已经学过实验室制取气体的一般思路和方法,请利用下列装置回答相关问题.
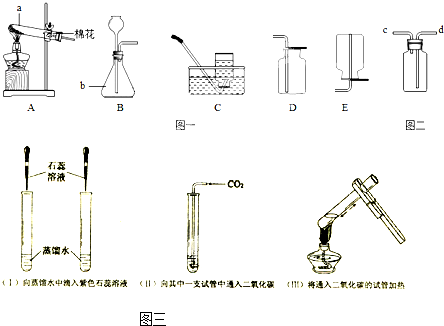
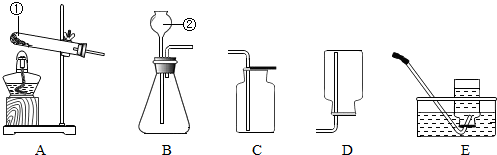
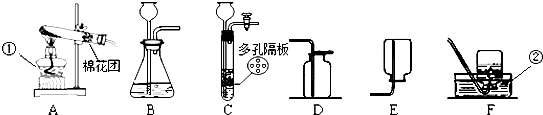
(1)写出图一中a和b的仪器名称:a
(2)选择图一中的装置制取和收集二氧化碳气体,那么应选择的装置是
(3)若要用图二装置收集二氧化碳气体,则气体应从
(4)用制取的二氧化碳进行如图3有关性质实验:
①实验3(Ⅱ)中溶液变
②实验3(Ⅲ)中加热之后,溶液又变为
(5)实验室用高锰酸钾制取氧气的化学反应方程式(或化学式表达式)
(6)同学称取一定质量的KMnO4固体放入大试管中,将温度控制在250℃加热制取O2.实验结束时,乙同学发现用排水法收集到的O2大于理论产量.针对这一现象,同学们进行了如下探究:
【提出猜想】猜想Ⅰ:反应生成的MnO2分解放出O2;
猜想Ⅱ:反应生成的K2MnO4分解放出O2;
猜想Ⅲ:反应生成的K2MnO4和MnO2分解都放出O2.
【实验验证】同学们分成两组,分别进行下列实验:
第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜想
第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是
【拓展延伸】实验发现,KClO3固体加热制取O2的反应速率很慢,但如果将KMnO4固体与KClO3固体混合加热,则KClO3的分解速率大大加快.请说明KMnO4在KClO3的分解反应中是否作催化剂,为什么?

(1)写出图一中a和b的仪器名称:a
试管
试管
; b锥形瓶
锥形瓶
;(2)选择图一中的装置制取和收集二氧化碳气体,那么应选择的装置是
B
B
和D
D
;在实验室中制取二氧化碳气体的常用药品:液体是稀盐酸
稀盐酸
,固体是石灰石或大理石
石灰石或大理石
.(3)若要用图二装置收集二氧化碳气体,则气体应从
d
d
(填c或d)端通.理由是二氧化碳的密度比空气大
二氧化碳的密度比空气大
.(4)用制取的二氧化碳进行如图3有关性质实验:
①实验3(Ⅱ)中溶液变
红
红
色;②实验3(Ⅲ)中加热之后,溶液又变为
紫
紫
色,解释出现此现象的原因加热后,碳酸不稳定而分解,溶液不再显酸性
加热后,碳酸不稳定而分解,溶液不再显酸性
.(5)实验室用高锰酸钾制取氧气的化学反应方程式(或化学式表达式)
2KMnO4
K2MnO4+MnO2+O2↑;
| ||
2KMnO4
K2MnO4+MnO2+O2↑;
若要用排水法收集一瓶较纯净的氧气,开始收集氧气的最佳时机是
| ||
气泡连续均匀冒出时收集
气泡连续均匀冒出时收集
.(6)同学称取一定质量的KMnO4固体放入大试管中,将温度控制在250℃加热制取O2.实验结束时,乙同学发现用排水法收集到的O2大于理论产量.针对这一现象,同学们进行了如下探究:
【提出猜想】猜想Ⅰ:反应生成的MnO2分解放出O2;
猜想Ⅱ:反应生成的K2MnO4分解放出O2;
猜想Ⅲ:反应生成的K2MnO4和MnO2分解都放出O2.
【实验验证】同学们分成两组,分别进行下列实验:
第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜想
Ⅰ
Ⅰ
错误;第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是
将带火星的木条放入试管内
将带火星的木条放入试管内
;【拓展延伸】实验发现,KClO3固体加热制取O2的反应速率很慢,但如果将KMnO4固体与KClO3固体混合加热,则KClO3的分解速率大大加快.请说明KMnO4在KClO3的分解反应中是否作催化剂,为什么?
高锰酸钾不是催化剂,加了高锰酸钾之后,产生氧气速度加快是因为高锰酸钾分解也会产生氧气,同时产生的二氧化锰对氯酸钾的分解起催化作用
高锰酸钾不是催化剂,加了高锰酸钾之后,产生氧气速度加快是因为高锰酸钾分解也会产生氧气,同时产生的二氧化锰对氯酸钾的分解起催化作用
.分析:(1)熟练掌握常见的化学仪器名称和用途;
(2)制取二氧化碳的药品是石灰石和稀盐酸,根据反应物的状态和反应条件选择发生装置,根据二氧化碳的密度和溶解性选择收集方法;
(3)根据二氧化碳的密度选择进气口;
(4)根据碳酸显酸性,能够使紫色的石蕊试液变成红色及碳酸不稳定,易分解,酸性消失,石蕊试液红色褪去又变成紫色分析;
(5)用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,写出反应的化学方程式;根据收集的方法和实验的注意事项分析;
(6)【实验验证】根据二氧化锰的质量不变,得出结论;
要验证猜想II,可以用验证氧气的方法来确定氧气的有无,可以用带火星的木条检验,观察现象;
【拓展延伸】根据高锰酸钾及氯酸钾反应的特点及催化剂分析回答.
(2)制取二氧化碳的药品是石灰石和稀盐酸,根据反应物的状态和反应条件选择发生装置,根据二氧化碳的密度和溶解性选择收集方法;
(3)根据二氧化碳的密度选择进气口;
(4)根据碳酸显酸性,能够使紫色的石蕊试液变成红色及碳酸不稳定,易分解,酸性消失,石蕊试液红色褪去又变成紫色分析;
(5)用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,写出反应的化学方程式;根据收集的方法和实验的注意事项分析;
(6)【实验验证】根据二氧化锰的质量不变,得出结论;
要验证猜想II,可以用验证氧气的方法来确定氧气的有无,可以用带火星的木条检验,观察现象;
【拓展延伸】根据高锰酸钾及氯酸钾反应的特点及催化剂分析回答.
解答:解:(1)a是试管;b是锥形瓶;故填:试管;锥形瓶;
(2)实验室制取二氧化碳的药品是石灰石或大理石和稀盐酸,属于固体和液体在常温下的反应,因此应选用的发生装置是B;因为二氧化碳易溶于水,密度比空气大,故收集装置D(向上排空气法);故填:B、D;稀盐酸;石灰石或大理石;
(3)因为二氧化碳的密度比空气大,会聚集在集气瓶的下方,故进气口是长管d;故填:d;二氧化碳的密度比空气大;
(4)二氧化碳与水反应产生碳酸,碳酸显酸性,能够使紫色的石蕊试液变成红色;碳酸不稳定,受热易分解,酸性消失,石蕊试液红色褪去又变成紫色;故填:红;紫;加热后,碳酸不稳定而分解,溶液不再显酸性;
(5)用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,因此反应的化学方程式为:2KMnO4
K2MnO4+MnO2+O2↑;用排水法收集气体的最佳时机是气泡连续均匀冒出时收集,这样收集的气体较纯净;故填:2KMnO4
K2MnO4+MnO2+O2↑;气泡连续均匀冒出时收集;
(6))【实验验证】取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,说明不是二氧化锰产生的氧气,故猜想Ⅰ错误;验证氧气的产生还可以用带火星的木条伸进试管内,看是否复燃;
故答案为:Ⅰ;将带火星的木条放入试管内;
【拓展延伸】加了高锰酸钾之后,产生氧气速度加快是因为高锰酸钾分解也会产生氧气,同时产生的二氧化锰对氯酸钾的分解起催化作用.
故答案为:高锰酸钾不是催化剂,加了高锰酸钾之后,产生氧气速度加快是因为高锰酸钾分解也会产生氧气,同时产生的二氧化锰对氯酸钾的分解起催化作用.
(2)实验室制取二氧化碳的药品是石灰石或大理石和稀盐酸,属于固体和液体在常温下的反应,因此应选用的发生装置是B;因为二氧化碳易溶于水,密度比空气大,故收集装置D(向上排空气法);故填:B、D;稀盐酸;石灰石或大理石;
(3)因为二氧化碳的密度比空气大,会聚集在集气瓶的下方,故进气口是长管d;故填:d;二氧化碳的密度比空气大;
(4)二氧化碳与水反应产生碳酸,碳酸显酸性,能够使紫色的石蕊试液变成红色;碳酸不稳定,受热易分解,酸性消失,石蕊试液红色褪去又变成紫色;故填:红;紫;加热后,碳酸不稳定而分解,溶液不再显酸性;
(5)用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,因此反应的化学方程式为:2KMnO4
| ||
| ||
(6))【实验验证】取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,说明不是二氧化锰产生的氧气,故猜想Ⅰ错误;验证氧气的产生还可以用带火星的木条伸进试管内,看是否复燃;
故答案为:Ⅰ;将带火星的木条放入试管内;
【拓展延伸】加了高锰酸钾之后,产生氧气速度加快是因为高锰酸钾分解也会产生氧气,同时产生的二氧化锰对氯酸钾的分解起催化作用.
故答案为:高锰酸钾不是催化剂,加了高锰酸钾之后,产生氧气速度加快是因为高锰酸钾分解也会产生氧气,同时产生的二氧化锰对氯酸钾的分解起催化作用.
点评:本考点主要考查气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关;在锰酸钾和二氧化锰是否会生成氧气探究中,有两个方案可以参考,质量变化法和生成物检验法,掌握氯酸钾和高锰酸钾的性质,理解催化剂的概念是解题的关键.

练习册系列答案
相关题目