题目内容
【题目】氯化钡是一种可溶性重金属盐,广泛应用于化工领域。用毒重石(主要成份为BaCO3)制备氯化钡晶体工艺流程如下: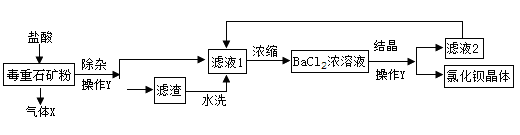
(1)毒重石要进行粉碎的目的是。气体X的化学式为。
(2)操作Y的名称是。该操作中用到的玻璃仪器有烧杯,玻璃棒和 , 其中玻璃棒作用__。滤液2中可循环利用的物质除水外还有。洗涤氯化钡晶体最适宜的洗涤剂是_(填字母)。
A.30℃水 B.30℃饱和氯化钠溶液 C.30℃饱和氯化钡溶液
(3)滤渣水洗的目的是_和_。
(4)取一定量的产物配成100 g 质量分数为5.2%的溶液,需要溶质的质量为__g,若量取水时俯视读数,则溶质质量分数将(填“偏大”、“偏小”“不变”)。
【答案】
(1)增大矿粉与酸接触面积使反应充分,CO2
(2)过滤,漏斗,引流,BaCl2(填名称也可),C
(3)提高原料的利用率(或提高产率),减少可溶性重金属钡盐对环境的污染
(4)5.2,偏大
【解析】(1)增大反应物的接触面积,可以加快反应速度,所以毒重石要进行粉碎的目的是加快反应速度;毒重石(主要成分为BaCO3)加入盐酸,盐酸与碳酸钡反应生成氯化钡、水、二氧化碳,所以气体是CO2;
(2)操作Y是将不溶于液体的固体和液体分离,所以是过滤;过滤操作时用到的玻璃仪器有烧杯,玻璃棒和漏斗,其中玻璃棒的作用是引流;滤液2是由氯化钡浓溶液通过结晶过滤得到的,所以滤液2中含有水、氯化钡;洗涤氯化钡晶体最适宜的洗涤剂必须能溶解杂质,但不能溶解氯化钡,所以要用30℃饱和氯化钡溶液清洗,不能溶解氯化钡,但能溶解其它杂质,可以将杂质洗掉,所以答案是C;
(3)滤渣水洗是为了将混在滤渣中的氯化钡回收,提高原料的利用率,减少可溶性重金属钡盐对环境的污染;
(4)需要溶质的质量为100g×5.2%=5.2g,若量取水时俯视读数,液面在刻度线下,水的体积偏小,则溶质质量分数将偏大。
所以答案是:增大矿粉与酸接触面积使反应充分、CO2、过滤、漏斗、引流、BaCl2(填名称也可)、C、提高原料的利用率(或提高产率)、减少可溶性重金属钡盐对环境的污染、5.2、偏大。

【题目】下列各选项中,解释与事实不吻合的是
选项 | 事实 | 解释 |
A | 打开汽水瓶盖时,汽水自动喷出 | 气体的溶解度随压强的减小而减小 |
B | 充气的篮球有弹性 | 分子间有间隔 |
C | 金刚石很坚硬,而石墨却很软 | 碳原子的排列方式不同 |
D | 酒精做温度计的填充物 | 酒精分子的体积大小随温度升降而改变 |
A.AB.BC.CD.D