题目内容
【题目】通过海水晒盐可得到粗盐,粗盐除NaC1外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如图。
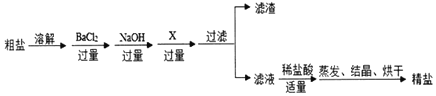
(1)加入过量BaC12溶液的目的是______(用化学方程式表示);
(2)加入试剂X的化学式是______。
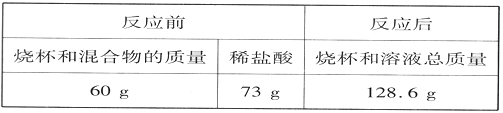
(3)实验所得精盐的质量______(选填“大于”、“小于”或“等于”)粗盐中氯化钠的质量。
【答案】Na2SO4+BaCl2=BaSO4↓+2NaCl Na2CO3 大于
【解析】
(1)硫酸根离子用钡离子沉淀,氯化钡与硫酸钠溶液反应生成硫酸钡沉淀和氯化钠,反应恶化学方程式为:Na2SO4+BaCl2═BaSO4↓+2NaCl;
(2)镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可溶液以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氯化钡溶液可以将硫酸根离子沉淀;至于先除镁离子,还是先除硫酸根离子都可以;钙离子用碳酸根离子沉淀,除钙离子加入过量的碳酸钠溶液转化为沉淀,但是加入碳酸钠溶液要放在加入的氯化钡溶液之后,这样碳酸钠会除去反应剩余的氯化钡,故试剂X是Na2CO3;
(3)碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳,故实验所得精盐的质量大于粗盐中氯化钠的质量。

练习册系列答案
相关题目