题目内容
【题目】高铁酸钾[K2FeO4]能溶于水,是高效、多功能水处理剂.
(1)K2FeO4中铁元素的化合价为 .
(2)如图所示,将K2FeO4溶于水,几天后振荡、静置,再滴入酚酞,出现如图所示现象.写出K2FeO4与H2O反应的化学方程式(其中K2FeO4与H2O的化学计量数之比为2:5) . 
【答案】
(1)+6
(2)4K2FeO4+10H2O═4Fe(OH)3↓+8KOH+3O2↑
【解析】(1)根据在化合物中正负化合价代数和为零,钾元素显+1,氧元素显﹣2,设铁元素的化合价为x,可知高铁酸钾(K2FeO4)中铁元素的化合价为:(+1)×2+x+(﹣2)×4=0,则x=+6.(2)将K2FeO4溶于水,几天后振荡、静置,再滴入酚酞,出现红褐色沉淀,说明有氢氧化铁生成,溶液变红,说明有碱氢氧化钾生成,气球变鼓,说明有气体氧气生成,反应的化学方程式为:4K2FeO4+10H2O═4Fe(OH)3↓+8KOH+3O2↑.
故填:(1)+6;(2)4K2FeO4+10H2O═4Fe(OH)3↓+8KOH+3O2↑.
【考点精析】掌握书写化学方程式、文字表达式、电离方程式是解答本题的根本,需要知道注意:a、配平 b、条件 c、箭号.

练习册系列答案
相关题目
【题目】NH4Cl和Na2SO4的溶解度表及溶解度曲线如图.下列说法正确的是( )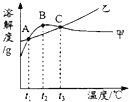
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度S/g | NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
A.甲为NH4Cl
B.t2℃应介于30℃﹣50℃
C.甲、乙饱和溶液从t3℃降温到t2℃,溶质的质量分数都变小
D.等质量的甲、乙饱和溶液从t1℃升温到t3℃,为使其溶液恰好饱和,加入的甲、乙固体质量相等