题目内容
【题目】某校化学兴趣小组的同学对实验室制氧气和氧气的某些性质进行了如下探究。已知图甲、图丙中装置的气密性良好。
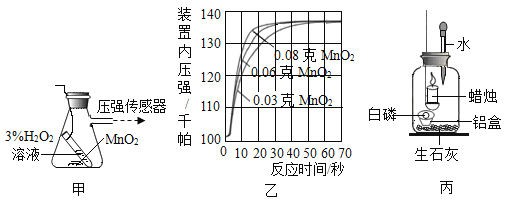
(实验探究1)利用图甲所示装置探究影响H2O2分解速率的因素,装置中产生氧气的量可以用压强传感器测出(在一定温度条件下,产生氧气的体积与装置内的压强成正比,反应放热忽略不计),得到图乙所示的图像。
(1)写出图甲装置中发生反应的化学方程式:_______。
(2)若三次所用的3%H2O2溶液都是8mL,从图乙中可以得出的两个结论是:
①________;
②_______。
(实验探究2)利用图丙所示装置探究氧气的浓度对燃烧的影响。点燃蜡烛后立即塞紧橡皮塞,待蜡烛熄灭后,将滴管中的水全部滴入瓶中,铝盒中的白磷立即燃烧。
(1)白磷燃烧的主要现象是________。
(2)由“蜡烛熄灭,白磷燃烧”可得出的结论是_______。
(3)滴入水后白磷立即燃烧的原因是______。
【答案】2H2O2![]() 2H2O+O2↑ 随所用二氧化锰的质量增加,反应速率加快 二氧化锰对生成氧气的量没有影响 放热、产生大量白烟 不同物质燃烧需要氧气的浓度不同 生石灰和水反应放热,使温度达到了白磷的着火点
2H2O+O2↑ 随所用二氧化锰的质量增加,反应速率加快 二氧化锰对生成氧气的量没有影响 放热、产生大量白烟 不同物质燃烧需要氧气的浓度不同 生石灰和水反应放热,使温度达到了白磷的着火点
【解析】
[实验探究1]
(1)图甲装置中发生反应的化学方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(2)若三次所用的3%H2O2溶液都是8mL,由图乙可知,当二氧化锰的用量不同时,压强达到最大值所需的时间不同,即随二氧化锰的质量增加,反应速率加快,但最终气体压强一样大,说明催化剂不影响最终生成氧气的量。
[实验探究2]
(1)白磷燃烧生成五氧化二磷,五氧化二磷是一种白色固体物质,同时放出热量,故反应的主要现象是放热、产生大量白烟。
(2)在同一容器中,由“蜡烛熄灭,白磷燃烧”可知,氧气的浓度低于一定值时不能支持蜡烛的燃烧,但可以支持白磷的燃烧,说明不同种物质燃烧所需氧气的浓度不同。
(3)滴入水后白磷立即燃烧的原因是生石灰和水反应放热,使与氧气接触的白磷的温度达到了着火点。

 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案【题目】中国“盐湖城”格尔木市举办世界钾盐钾肥大会,我国将成为世界第四大加盐钾肥生产国。下表是重要钾盐氯化钾在不同温度下的溶解度(单位:g/100g水)
温度/℃ | 20 | 40 | 60 | 80 |
KCl溶解度 | 34.0 | 40.0 | 45.5 | 51.1 |
某化学兴趣小组同学在20℃的l00g水中进行了如图所示的实验,请据图回答问题:
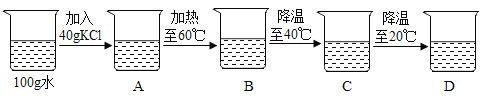
(1)从表中数据可以看出氯化钾的溶解度随温度升高而_____(填“增大”或“减小”);
(2)图中烧杯A中所得到的溶液属于_____(填“饱和”或“不饱和”)溶液,溶液质量为___g;
(3)图中烧杯B中的溶质质量分数为___________;
(4)图中烧杯C和D中的溶液相同的是 __________(填序号)
①溶质的质量 ②溶剂的质量 ③溶液的质量 ④溶质的质量分数