��Ŀ����
����Ŀ����1���ϸ���ָʾ����������:
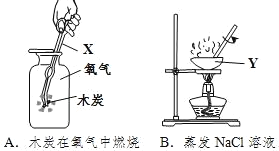
ʵ�������õ���ҩƷ�����������ڼ�������ҵ����Ʒ���밴Ҫ����ա���ȡ200g�ϸ���˺��(ȥ����)������500mLˮ���м���200mLˮ���ڼ���ե֭�����飬��ʵ�����з���___________(����������)�е��á��ڼ���Ũ��Ϊ50%�ƾ����ݣ���ͥ����____________���棬������˫��ɴ�����ˣ����ã�ȡ�ϲ���Һ������ɫ���ϸ���ɫ����Һ��
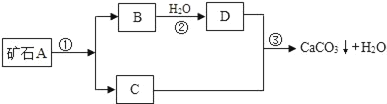
(2)�����Na2O2����֬���д�������֬��ȼ����������֪:![]()
Na2O2��һ�ֵ���ɫ���壬����������CO2��H2O��HCl��������ʷ�Ӧ������O2��������N2��Ӧ��
ʵ��:���봿���������N2һ��ʱ�����ͨ����� CO2���۲쵽��֬����ȼ�ա���֤Na2O2����CO2��Ӧ���ͷų�����
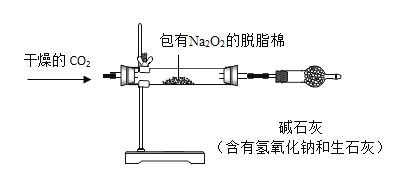
��ͨ�봿�������� N2��Ŀ����______________________________����ʯ�ҵ�������__________________��
�ڸ÷�Ӧ������һ���� A����Ӧ�Ļ�ѧ����ʽ��___________________����46g�Ƶ�����ȫ��Ӧ�ܲ���__________________g��A��
���𰸡��в� ��Ũ�Ȱ� �ų�����������������Ʒ�Ӧ������ ��ֹ����������������Ʒ�Ӧ��������� 2Na2O2+2CO2==2Na2CO3+O2 106
��������
��1����ȡ200g�ϸ���˺��(ȥ����)������500mLˮ���м���200mLˮ���ڼ���ե֭�����飬��ʵ�����з����в��е��á��ڼ���Ũ��Ϊ50%�ƾ����ݣ���ͥ���ø�Ũ�Ȱƴ��棻
��2���ٸ��ݡ�NaO2��һ�ֵ���ɫ���壬����������CO2��H2O��HCl��������ʷ�Ӧ������O2��������N2��Ӧ����֪��ͨ�봿�������� N2��Ŀ�����ų�����������������Ʒ�Ӧ�����壻��ʯ�ҵ������Ƿ�ֹ����������������Ʒ�Ӧ��������룻
�ڸ��ݡ�Na2O2��һ�ֵ���ɫ���壬����������CO2��H2O��HCl��������ʷ�Ӧ������O2��������N2��Ӧ���������غ㶨�ɿ�֪���÷�Ӧ������һ���� A��̼���ƣ���Ӧ�Ļ�ѧ����ʽ��2Na2O2+2CO2==2Na2CO3+O2��
���������غ㶨�ɿ�֪��̼�����е���Ԫ����������46g���ɴ˲���̼���Ƶ�����=![]() ����46g�Ƶ�����ȫ��Ӧ�ܲ���106g��A��
����46g�Ƶ�����ȫ��Ӧ�ܲ���106g��A��

 53���ò�ϵ�д�
53���ò�ϵ�д�����Ŀ������г����������ҵ�г��õ�����Ư����
���� | �������� | �������� | Ư�� |
��ѧʽ | NaClO2 | ClO2 | Ca(ClO)2��CaCl2 |
(1)����Ư���У�Ca(ClO)2����___(�����)��
�ٻ���� �ڻ����� ��������
(2)ClO2����Ԫ�صĻ��ϼ�Ϊ___��
(3)�����е�����(��CaCl2)����Ԫ�ص���������������___��
(4)�������[Ca(ClO)2]��Ư�۵���Ч�ɷ֣�
�ٴ�������ڳ�ʪ�Ŀ����о��û����ɾ���Ư���Ե����ʴ�����(HClO)��������ˮ�İ�ɫ���壬��Ӧ�Ļ�ѧ����ʽ___���÷�Ӧ�Ļ���������___��
�ڹ�ҵʹ��Ư��ʱ������(4)�Тٵķ�Ӧԭ����ͨ������������___(�����)���������Ư��Ư���������⣮
A �������� B ϡ���� C �������� D �Ȼ��ƣ�
����Ŀ���ճ������У���������̼������Һ���м��ԣ���ϴ�;��ϵ����ۣ�����Խǿ��ȥ���۵�Ч��Խ�á�����ʵ����Ӱ��̼������Һ���Ե�����չ��̽������̼���ƹ���Ͳ�ͬ�¶ȵ�ˮ�������������������ֱ�Ϊ 2%��6%��10%��̼������Һ������������Һ��pH����¼���±�:
ʵ���� | �� | �� | �� | �� | �� | �� | �� | �� | �� |
������������ | 2% | 2% | 2% | 6% | 6% | 6% | 10% | 10% | 10% |
ˮ���¶�/��C | 20 | 40 | 60 | 20 | 40 | 60 | 20 | 40 | 60 |
��Һ pH | 10.90 | 11.18 | 11.26 | 11.08 | 11.27 | 11.30 | 11.22 | 11.46 | 11.50 |
��1��ȥ���۵�Ч����õ���___________ (��ʵ����)��
��2�� ��һ���¶ȷ�Χ�ڣ��¶ȶ�̼������ҺpH��Ӱ����:��_______��ͬʱ��______��
��3�����ijʵ��С����õ����õ�ȥ��Ч��������֮ǰ��ʵ����ɣ����Գ��Ե�ʵ��������__________________
A 12%�� 60��C B 8%�� 40�� C C 10%�� 70��C
��4��̼������Һ�ʼ��Ե�ԭ���ǣ�һ����̼�������ˮ�����̼��������Ӻ����������ӣ��ٲ���̼���������ˮ�����̼������������ӡ�����100g10%̼������Һ��̼Ԫ�ص�������_________g(��ȷ��0.1)