题目内容
我市某厂高温煅烧石灰石制生石灰,每天需要含碳酸钙80%的石灰石原料100t ,假设杂质受热不分解。请计算:
⑴理论上每天可生产氧化钙多少吨?产生二氧化碳多少吨?
⑵煅烧后的产品中氧化钙的质量分数。(计算结果精确到0.1%)
⑴理论上每天可生产氧化钙多少吨?产生二氧化碳多少吨?
⑵煅烧后的产品中氧化钙的质量分数。(计算结果精确到0.1%)
(1)氧化钙:44.8t 二氧化碳:35.2t (2) 69.1%
(1)根据混合物中组成物质的质量=混合物的质量×该组成在混合物中的质量分数,由含碳酸钙80%的石灰石原料100t计算出碳酸钙的质量;然后根据反应的化学方程式,由碳酸钙的质量计算生成氧化钙,二氧化碳的质量;
(2)煅烧后的产品为含杂质的氧化钙,其质量为煅烧所生成氧化钙的质量与受热不分解的杂质质量和,由生成氧化钙的质量与含有杂质的氧化钙的质量比可计算煅烧后的产品中氧化钙的质量分数.
CaCO3="=" CaO+CO2↑
100 56 44
100t*80% x y
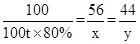
x=44.8t y=35.2t
CaO%=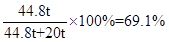
(2)煅烧后的产品为含杂质的氧化钙,其质量为煅烧所生成氧化钙的质量与受热不分解的杂质质量和,由生成氧化钙的质量与含有杂质的氧化钙的质量比可计算煅烧后的产品中氧化钙的质量分数.
CaCO3="=" CaO+CO2↑
100 56 44
100t*80% x y
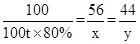
x=44.8t y=35.2t
CaO%=
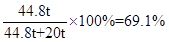

练习册系列答案
相关题目
 2 KCl + 3O2↑)
2 KCl + 3O2↑) 4Al + 3O2↑。如果加工一个铝锅需要1.08 Kg的铝,至少需要电解多少质量的氧化铝才能制成这个铝锅?
4Al + 3O2↑。如果加工一个铝锅需要1.08 Kg的铝,至少需要电解多少质量的氧化铝才能制成这个铝锅?